A szilárd fázisú - kristályosítással elmélet - studopediya
szilárdanyag képződéshez (kristályosítás) - egy összetett folyamat, amely több szakaszból áll.
1. Kiszáradás ionok miközben egy csapadék képződik. Hidratált ionokat oldatban, szilárd fázisú, sok esetben, nem tartalmaz vizet, azonban ionokat alkotnak egy kristály kell veszíteni hidratációs vizet.
2. A formáció primér magok. Két ionok ellenkező előjelű, együtt a molekula nem képeznek egy másik kristályos formát. A formáció a primer krisztallit áthalad egy sor közbenső lépések. Ily módon, amikor a bárium-szulfát csapadék túltelített oldatok az ilyen folyamatok fordulnak elő:
Ba 2+ + SO4 2- Ba 2+ ↔ SO4 2- - ionpár képződését;
Ez az úgynevezett indukciós periódust.
Így, hogy egy primer kristályt bármely pont a megoldás kell kombinálni egymással legalább néhány ionok ellenkező előjelű. Csak ebben az esetben alkothat egy primer kristály (embrió), mint például egy kocka alakú.
3. Növekedési elsődleges gócképződés által letétbe őket a növekvő ionok mennyiségét, ami a nagyobb kristályok képződése, kombinálásával nagyobb aggregátumokká, nem alkalmas, azonban még mindig kiemelkedik az oldatból csapadék formájában. Ez - kolloid szakaszában képződését oldhatatlan vegyületek.
4. Formation egy ideig az oldatban olyan nagy kristályok vagy aggregátumok. hogy azok már nem oldatban tartható, és végül szabadul szilárd fázis (csapadék).
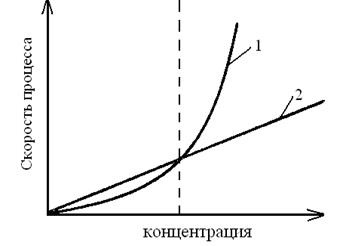
Ábra. 3.1. A függőség gócképződési sebesség (1)
a növekedés és a (2) a relatív túltelítettség
A kapott csapadékot eltérhetnek azok tulajdonságait. Egyes esetekben, megkülönböztetni amorf csapadékok, másokban - kristályos.
A természet a csapadék függ a sebesség aránya két folyamat: gócképződési sebességet - primér magok # 965; 1, és a mérete a sejtmagok növekedési ráta # 965; 2. jelentés # 965; 1 és # 965; 2 viszonyítva definiáltuk túltelítettség előforduló hozzáadásakor kicsapószer oldatot.
Mérték oldatot túltelítettség foka túltelítettséget R, amely úgy definiálható, a következő kifejezéssel:
ahol C a koncentráció letétbe helyezett anyag, amelyet úgy kapunk, bevezetésével a kicsapószer képzésére;
S - egyensúlyi oldhatósága a csapadékot ilyen körülmények között
Jellemzően a kis értékei a relatív túltelítettség # 965; 2> # 965; 1 növeljük sebességét mindkét folyamat valamikor egyenlő, és végül sebesség # 965; 1 kezd érvényesülni, vagyis .. # 965; 2 kisebb lesz # 965; 1.
Ábra. 3.1 azt mutatja, hogy a kis értékei esetén a relatív túltelítettség (bal oldali részén az ábrán) dominál a gócképződés sebessége növekedés és magasabb értékeket (a jobb oldali részén az ábrán) dominál a képződési sebességét új magok.
Tekinteni attól, hogy miért bizonyos esetekben amorf formájú, és mások - kristályos kiválás.
Amikor egy új, kicsapó oldatot egy első időpontban képződik túltelített oldatát oldható anyag. Ha az anyag lassan oldódik, azt érjük el, nagy relatív túltelítettség és a gócképződés sebessége jóval nagyobb, mint a növekedési ütem. Ilyen körülmények között, hozzáadása után következő részeiben kicsapó oldattal, a nagyszámú új kristályosítási központok. Ezek az elsődleges embriók egyesülnek nagyobb aggregátumokká, és elválasztjuk az oldatból, mint egy amorf csapadék.
Ezzel szemben, ha a az anyag oldhatóságát nem túl kicsi, a relatív túltelítettség kisebb, mint az első esetben, és az adagolás után a kicsapó oldat keletkezik viszonylag kis magok, amelynek méretei gyorsan növekszik. A oldatot osztják egyes kristályok inkább jelentős méretű - kristályos csapadékot kapunk.
Amorf betétek állnak több lazán kapcsolódik nagyon kis kristály. A legtöbb ilyen betétek egy olyan kristályos szerkezettel, amellyel ők is nevezik kriptokristályos.
A túltelítettség foka az oldat lehet változtatásával változtatható leválasztási körülmények.
Durvára csapadékot előnyösebb, mint kis kristály, és különösen egy amorf csapadék. Feltételei lerakódás lehetséges meghatározni, hogy az értéke a túltelítettség foka az oldat: egy kristályos csapadék képződik, szükséges, hogy csökkentsék a túltelítettség foka R.
Szerint általános képletű (3,1), hogy csökkentsék a szükséges koncentráció csökkentésére R A letétbe helyezett anyag (C) és az oldhatóság növelése érdekében (S).
Koncentrációjának csökkentésére a vegyület kell letétbe lehet elérni:
1) szerinti oldatot;
2) koncentrációjának csökkentése a kicsapószert ( „eredő reagens” módszer) vezetünk be egy oldatot egy anyag, amely, adott esetben a reakciót általában fut kis sebességgel, kiválaszt egy kívánt kicsapószer oldatot.
Fokozott oldhatóságának a csapadékot a csapadék úgy érjük el a hőmérséklet növelésével vagy hozzáadásával elektrolitok, amelyek növelik a só hatása.
A legfontosabb jellemzője, amorf csapadék nagyon nagy közös felszíni. Ebben a tekintetben a felülete amorf csapadékok gyakran adszorbeálja idegen anyagot. Továbbá, mivel a nagy számú igen kis egységek, amelyek rosszul csatlakoztatva, mosásával az amorf csapadékot képezhet kolloid oldatokat.