Nyugtalan láb szindróma
Az RLS felnőttek körében előforduló gyakoriság 5-15%, átlagosan 10%. Az RLS gyakoribb Észak- és Nyugat-Európában, sokkal ritkábban az ázsiai országokban és Dél-Európában. Valamivel gyakrabban RLS található a nők körében, valamint a 65 évnél idősebbeknél. Elfogadható az elsődleges és a másodlagos RLS kiosztása. Ezek a populációban ugyanolyan gyakorisággal fordulnak elő.
Az elsődleges SBN etiológiája ismeretlen, neurológiai és szomatikus betegségek hiányában, fiatalabb, néha gyermekkorban. Az elsődleges RLS esetek körülbelül 92% -ánál a családi történelem súlyosbodott családi előzménye. Tegyük fel, hogy az autoszomális domináns típusú öröklődés magas penetrációval bír. Néhány családban kiderült, hogy a 9., 12. és 14. kromoszómákban az RLS és a lokuszok társulnak.
A másodlagos RLS általában 50 év után fordul elő számos szomatikus és neurológiai betegség hátterében.
A másodlagos RLS szomatikus okai:
- vasveszteség, B12 és folsavhiányos anémia;
- veseelégtelenség;
- a pajzsmirigy rossz működése (hipotireózis, hyperthyreosis);
- krónikus obstruktív tüdőbetegség;
- ízületi betegségek;
- az alsó végtagok edényeinek elváltozása;
- az alsó végtagok vénás keringése.
A másodlagos RLS neurológiai okai:
- polyneuropathia (alkoholizmus, cukorbetegség, amyloidosis, porphyria, örökletes szenzomotoros neuropátia);
- gerincvelő sérülések (tumor, trauma, spinális érzéstelenítés, sclerosis multiplex, myelopathia, myelitis, amyotrophic lateral sclerosis);
- diszkogén radiculopathia;
- Parkinson-kór;
- Huntington-kór:
- esszenciális tremor.
A másodlagos RLS orvosi okok a következők:
- antidepresszánsok (triciklikus antidepresszánsok, szerotonin visszavétel gátlók);
- lítiumkészítmények;
- antipszichotikumok, antiemetikumok (metoklopramid);
- antihisztaminok;
- kalcium antagonisták és β-blokkolók.
Másodlagos RLS is előfordulhat terhesség alatt, a koffeint tartalmazó italokkal való visszaéléssel, valamint jelentős fizikai megterhelés után.
Az RLS patogenezise nem teljesen ismert. Az általános és a másodlagos RLS fejlesztésének általános mechanizmusai feltételezhetők. Az RLS három fő patogenetikai tényezője összefügg egymással:
- dopaminerg diszfunkció;
- a vas homeosztázis megsértése;
- genetikai mechanizmusok.
Dopaminerg diszfunkció az RLS patogenezise központi szerepe van, főleg a csökkenő dopaminerg diencephalikus-gerincvelői előrejelzések, amelyek forrása a dopaminerg neuronok a caudalis részén a talamusz, a hipotalamusz és közép agyi szürkeállomány körül az agyi vízvezeték. Az egyik elmélet fejlettségi RLS vállalja a szerepét, megsértése supraspinalis fájdalom modulációs mechanizmusok közé tartozik az bazális ganglionok és a lemenő dopaminerg utat. A szerepe diszfunkció a dopaminerg rendszer patogenezisében az RLS-tünetek csökkenése is megerősíti a találkozó dopaminergiás szerek (dopamin receptor agonisták és a levodopa készítmények).
Számos kutató tudomásul veszi a vas-anyagcsere szerepét az extrapiramidális rendszerben az RLS-ben. A vas az enzim kofaktora, amely részt vesz a dopamin szintézisében; Ezenkívül a vas része a dopamin receptorok fehérje szerkezetének.
Az RLS áram
A életkorban alakul primer RLS változó: a betegek korai kezdetű a betegség (50 éves) tünetek jelentkeznek fokozatosan, míg a betegek késői bemutatkozó (50 év után), van egy gyorsabb áramlást. Általában jegyezni krónikus helyhez kötött vagy lassan progrediáló természetesen romlása javulási és stabilizálása a tünetek. A károsodások elsődleges RLS is kiválthatja fizikai megterhelés, stressz, a beszívott dopamin receptor blokkolók, antidepresszánsok és a koffein visszaélés, a dohányzás, az alkohol. A másodlagos RLS lefolyása az alapbetegségtől függ.
Differenciáldiagnosztika
RLS meg kell különböztetni a éjszakai görcsök, akathisia, éjszakai myoclonia, polineuropátia, obliteratív érbetegség az alsó végtagok.
RLS kezelése
Amikor elsődleges és másodlagos RLS-t ajánlunk a dohányzásról való leszokáshoz, használjunk koffeintartalmú italokat, alkoholokat. Alvási higiénia ajánlott (bizonyos ideig alvás, esti séták, meleg zuhany), lábmasszázs, nagyon meleg vagy nagyon hideg lábfürdő, mérsékelt fizikai aktivitás, a napi rutin normalizálása. A fizioterápia, a reflexoterápia csak bizonyos esetekben határozott pozitív hatással bír. A gyógyszerterápia elrendelésére vonatkozó döntésnek számos tényezőt kell figyelembe vennie: a tünetek súlyossága, a fájdalom szindróma jelenléte, az alvászavarok, az életminőség és a beteg napi aktivitása.
Az RLS kezelésének általános terápiás megközelítései a következők:
- Mégsem gyógyszerek, amelyek ronthatja SC (a dopamin receptor antagonisták, antidepresszánsok, lítium-gyógyszerek, antihisztaminok, kalcium-csatorna blokkolók, (β-blokkolók).
- A fő szomatikus és neurológiai betegség kezelése másodlagos RLS-ben.
- Figyelembe véve a beteg korát és a farmakoterápia mellékhatásainak kockázatát.
- Figyelembe véve az RLS súlyosságát és annak az alvásra gyakorolt hatását és a beteg életminőségét.
- A gyógyszer dózisának, gyakoriságának és idejének meghatározása.
- Terápia beindítása minimális terápiás dózisokkal.
- A dózis lassú titrálása fokozatosan a minimális hatékonyság érdekében.
- A kombinációs terápia érvényességének értékelése, ha a monoterápia hatástalan.
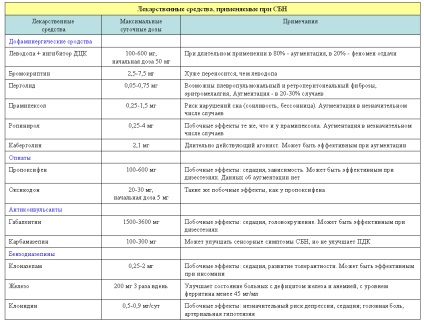
Az RLS farmakoterápiáját a betegség progresszív folyamata, az álmatlanság, a nappali álmosság és a betegek napi aktivitásának és életminőségének romlása jellemzi; átlagosan a betegek mindössze 20-25% -a szükséges. Az RLS-re előírt legfontosabb gyógyszerek a dopaminerg készítmények. görcsoldók. benzodiazepinek. onoids (lásd a táblázatot).
A dopaminerg gyógyszerek (dopamin receptor agonisták, levodopa) a legelterjedtebbek az RLS-ben, és az elsődleges gyógyszerek az elsődleges és a másodlagos szindrómák kezelésére.
A levodopa használata esetén egy 1987 sc g. Levodopát kombinálva adjuk be egy DOPA dekarboxiláz inhibitor - MCM (benszerazid vagy karbidopa) dózisban 50 mg 1 óra előtt aludni, míg az ezt követő a hatásosság hiánya adag nőtt 100-200 mg. Azonban, két fő szövődmények elhúzódó levodopaterapii figyelhető meg az RLS kezelésében - augmentációs (tünetek fokozódása), és a jelenség a visszarúgás. visszarúgás jelenség fordul elő 46% -ában 6 hónapon belül folyamatos használat 160 mg levodopa. Ez nyilvánul meg a tünetek visszatérnek, a második felében az éjszaka vagy kora reggel, miután az esti fogadás levodopa. A jelenség a hatást csökkenteni lehet hozzárendelés meghosszabbított formáihoz levodopa késleltetett felszabadulását a hatóanyag vagy vételére további dózisok a levodopa a visszatérő tüneteket. Az augmentáció az RLS súlyosságának és a tünetek korábbi megjelenésének a növekedése során jelentkezik. Ez a jelenség az esetek 80% -ában 2 hónap után alakul ki. levodopa alkalmazása RLS-ben.
Az augmentáció fejlesztésekor:
- ellenőrizze a ferritin szintjét a plazmában, és szükség esetén írja elő a vaskészítményeket
- csökkentse a levodopa adagját, vagy szétfeszítheti a levodopát
- írjon elő egy levodopa további bevitelt egy korábbi időpontban
- adjunk agonistákat a dopaminreceptorok (ADAP) vagy teljesen váltsunk át levodopáról az ADAR-ra
- helyettesítse a dopaminerg szereket antikonvulzív szerekkel, benzodiazepinekkel.
Az augmentáció sokkal kevésbé gyakori az ADAP kinevezésével - legfeljebb az esetek 20-30% -ában.
Az ADAR jelenleg az RLS kezelésének legfontosabb eszköze. Ezek befolyásolják az MPC-t, csökkentik a paresztézia és dysesthesia súlyosságát, normalizálják az alvást. ADAR felhasznált acél RLS 1988 A hatékonyság hasonló a levodopa, de a hosszú távú terápia sokkal kevésbé valószínű mellnagyobbítás és rebound jelenség. Még alkalmasabban rendelni neergolinovye agonisták (pramipexol, rotigotin), mivel ezek nem rendelkeznek a súlyos mellékhatások, mint a retroperitonial- ny, szelep és a tüdőfibrózis, amelyek néha megnehezítik terápiát ergolinovymi származékok (bromokriptin, kabergolin). ADAR hatásos SC dózisok lényegesen alacsonyabbak, mint azok, alkalmazni, amikor Kinson Parkinson-kór, és így a mellékhatások kockázata, ha használják sc, általában is valamivel alacsonyabb.
A Pramipexole egy unergolin dopamin agonista, amely nagy szelektivitást mutat a D2 - AND D3 receptor altípusokra. A pramipexol magas biológiai hasznosíthatósággal rendelkezik (90%), felezési ideje a plazmában 8-12 óra.
A pramipexol csökkenti az érzékszervi és a motoros megnyilvánulásokat, az RLS súlyosságát, javítja az objektív és szubjektív alvási mutatókat. A poliszomnográfiai vizsgálatok szignifikáns csökkenést mutattak az MPC indexben, javították az alváshatékonyságot és növelték annak időtartamát. A pramipexol hatásosságát egyetlen esti dózis beadása és hosszantartó terápia után igazolták. A Pramipexol-ot 0,125 mg dózisban adják be 2 órával az RLS kezdeti ideje előtt, majd szükség esetén fokozatosan növelje a dózist 0,125 mg-mal 2-3 naponként egyszer vagy kétszer a terápiás hatás eléréséig.
A kezdeti dózis és dózis titrálási séma a beteg életkorától és súlyosságától függ. Például fiatal, magas intenzitású RLS-ben szenvedő betegeknél a kezdeti adag 0,25 mg lehet, majd 2 naponként megemelkedik. Ugyanakkor idős betegeknél a pramipexol kezdő adagja 0,125 mg, lassabban növekszik - hetente egyszer. Általában a pramipexol hatásos dózisa RLS-ben nem haladja meg a 0,5 mg-ot.
A dopaminerg szerek, az antikonvulzív szerek elégtelen hatékonyságával a benzodiazepinekre van szükség. Az opioidokat általában súlyos RLS-ben alkalmazzák súlyos fájdalom-szindrómás betegeknél, nappali tünetekkel; valamint egyéb gyógyszerek hatástalansága esetén.
Az RLS kezelését néha csak a megnövekedett tünetek időszakában végzik, de a legtöbb esetben az elsődleges RLS-kezelés hosszú ideig, néha az egész életen át történik. A dopaminerg terápia a leghatékonyabb az RLS-ben, és további diagnosztikai kritériumként használható fel erre a betegségre. A SBN első terápiás gyógyszerei az ADAR.