Celluláris onkogének, mint a rák kialakulásának okai
Celluláris onkogének, mint a rák kialakulásának okai
A megértése rendellenességek szabályozási folyamatok tumorsejtekben, jelentősen hozzájárult t tett a közelmúltban felfedezett DNS-szekvenciák a genotípusok a tumoros és normál sejteket, amelyek homológ virális onkogének. Az "onkogén" kifejezés nem lehet a legsikeresebb, mivel rosszindulatú transzformációra utal vagy az egészséges gének abnormális aktiválódását vagy a túlzott expresszióhoz vezető génkárosodást jelenti.
Ebből a szempontból ezek a gének nem rákgének, hanem csak proliferatív génszabályozók. Az utóbbi szabályozási funkciója megszakadhat, ami rákos daganat kialakulásához vezet, ideértve annak invázióját és áttétét.
Jelenleg számos olyan gént azonosítottunk, amelyek homológok DNS bizonyos régiói számára. kódolt retrovírusok. A gének ezen csoportjának különböző betegségekre gyakorolt hatásmechanizmusa változik. Tehát a Burkita lymphoma esetében a 8. kromoszóma részének kölcsönös transzlokációja a 2., 14. és 22. kromoszómákkal történik. Emellett sok esetben a 8. és 14. kromoszómák transzlokációját határozzuk meg.
Az onkogén c-myc a 8-as kromoszóma transzpozált régiójában helyezkedik el, és a transzlokáció alatt szerkezete átalakul. A krónikus granulocitás leukémia (HGL) onkogén c-abi-svom transzlokációs partnere gén bcr, generál egy fehérje-komplex képződését, ami az enzim expresszióját tirozin kináz - stimulátor sejtosztódást. Ebben az esetben csak a proto-onkogén aktiválása a legtöbb esetben nem vezet a rák kialakulásához.
Természetesen a CHL fejlődése agresszívabb leukémiás formákban további mutációkat igényel. Fokozott expressziója celluláris onkogének találtuk számos humán rákos sejtvonalakban: ez a gén expresszióját c-myc, a tenyészetek a kis-sejtes tüdőrák, és a Burkitt-limfóma, és N-gén-myc neuroblastoma. Nagyon gyakran a c-KIT gén mutációi vannak a gastrointestinalis traktus (OLCT) daganataiban. Ez az onkogén homológ a macska fibrosarkó vírus génjével (v-KIT). Ez a gén kódolja egy receptor termelését egy sejtnövekedés-stimuláló szerhez, egy tirozin-kinázhoz.
Egy tirozin-kináz antagonista. amelyet a krónikus granulocita leukémia fokozott aktivitásának blokkolására fejlesztettek ki, szintén gátolja a c-KIT gén expresszióját, ami a daganat regressziójához vezet.
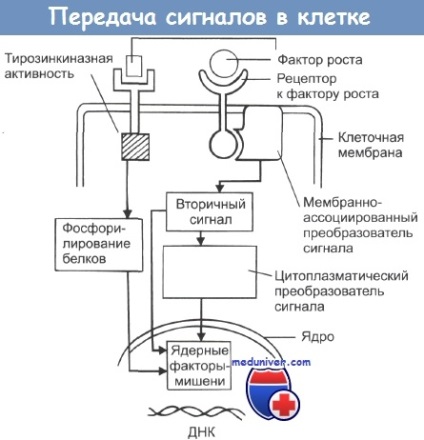
Az ábra egy egyszerűsített rendszert mutat be. A növekedési faktor a sejt membrán receptorához kapcsolódik. A receptor aktiválja a jelfehérjét, amely ezután kötődik guanin-nukleotid molekulákhoz (ebben a szakaszban G-fehérje). A G-protein jelmolekulái stimulálják egy szekunder hírvivő, például ciklusos adenozin-3 ', 5'-foszfatáz aktivitását. Egy alternatív aktivációs mechanizmusa plazma részét a receptor tirozin kináz aktivitását lehet kezdeni, ami foszforilációját tirozin bázisok intracelluláris proteinek, amelyek közül néhány stimulátor a sejtnövekedés és induktor Division.
A jelenleg ismert számos onkogént és származékát a táblázatban mutatjuk be. Onkoprotein c-erb B1, ami a receptor EGF, tartozik egy osztály receptor tirozin-kinázok (ez a csoport magában foglalja a HER2 / neu (erbB2), ErbB3 vagy ErbB4). Az EGF kötődése a receptorhoz (ligandumként) megindítja a tirozin-kináz aktivitását, ami a sejtfehérjék foszforilezéséhez vezet.

Az EGF-receptor komplexben a rákban fellépő hiperexpresszió vagy mutagén károsodás fokozza a receptor aktivitását. A fő cél az intézkedés az az EGF-receptor komplex a ras-patkány-MAP kináz, protein-kináz kaszkád Jak / Csillagok reakciók és a PI-3-kináz-útvonal. Számos modern gyógyszer hatása éppen az ilyen kaszkádreakciók gátlására irányul, és a monoklonális antitesteket úgy tervezték meg, hogy blokkolják a receptort.
A membránreceptor fehérjék kötődhetnek a guanozin 5'-trifoszfatázhoz (GTP), és a GTP-ase aktivitás leállítja a receptorok jelzését. A defektív G-fehérje, amelyet a mutált ras-onkogén kódol, gátolja a GTPáz aktivitását, és nem tudja abbahagyni a sejtek jelzését időben. A ras-onkogének családja három tagból áll (H-ras-1, K-ras-2, N-ras) és számos más, részben homológ fehérjét
A sejttenyészetekben az in vitro ras-protein okozza a fibroblasztok rosszindulatú transzformációját, kifejeződése szintén az embrionális fejlődés során a sejtek differenciálódásához kapcsolódik.