Ha az oxidációs szint növekszik a kémiai reakció során, azt mondják, hogy oxidált
Ezek a szabályok hasznos sok esetben. Lásd például, c könnyen meg lehet határozni keresztül oxidációs állapotban változó elem (vagy ismeretlen) vegyérték-molekuláris képlete. Tegyük fel, hogy van kapcsolat H2 SO3. A kérdés az, hogy mi az oxidáció mértékét a kén? Mivel az oxidáció mértékét hidrogén mindig (1), és az oxidáció mértékét az oxigén (-2), akkor könnyen kiszámítható, hogy a pozitív és negatív oxidáció mértékét „egyensúly” egymást a molekula H2 SO3, amikor a mértékét a kén oxidáció (4). Ebben az esetben, az algebrai összege valamennyi oxidációs fokú a molekulában nullával egyenlő:
A működését ez a szabály is mutatja a példa a reakció kén oxigénnel, amelyben elektronok formálisan az egyik atom a másikra:
A reakció előtt az oxigén és a kén, azonos - a nulla oxidációs állapotú. A reakció növelte a fokú kén oxidációs (4). Ennélfogva, a kén-oxidok.
Az oxidáció mértéke csökkent oxigén (-2), azaz az oxigén kinyerjük. Az algebrai összege minden fokú oxidáció SO2 maradt nulla.
Hasonló reakciók az oxidáció mértékét a reagáló atomok - egy hatalmas készlet. Együtt nevezik őket redox reakciókat.
A következő fejezetekben fogjuk vizsgálni ezeket a válaszokat részletesen, és még egyszer meg fogjuk érteni az új feltételeket.
Ahogyan nehéz emlékezni, amit a folyamat - vagy visszahatás elektronbefogás - az úgynevezett oxidációs, és amely - hasznosítás. Mit jelent negatívvá válik, és néhány - pozitív oxidációs állapotban van.
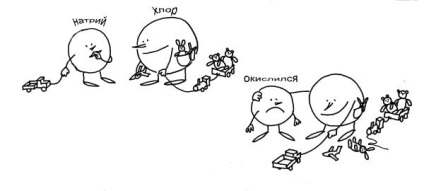
Ábra. 3-11. Nem egészen szokásos utáni kémiai reakció egyenlete: Na + Cl = NaCl (lásd a szöveget.). Klór - „negatív”, ő választja ki a többiek elektronokat. Nátrium „oxidált” - nyilvánvaló az ő savanyú arccal.
Ahhoz, hogy néhány, akkor kitalálni. 3-11-ba, amely a reakció a nátrium és a klór, mintha történt „kémiai óvodában.” Ez a „gyerekszobában” megrendelések ugyanazok, mint a hagyományos. A klór játékok, mint 7 (elektron). Nátrium ugyanaz van csak targonca (1 elektron). Klór akkor látta, hogy egy teherautó nátrium és úgy döntött, hogy ezt a játékot, és ez nem elég! Klór is erősebb, így a teherautó azonnal elfordult tőle. És nem köcsög Nátrium (van egyfajta oxidok!), Klór kínált együtt játszani. Mi is ott van! Természetesen mind a 8 játék Klór húzta közelebb hozzá, és a nátrium csak az maradt hátra, hogy álljon mellé a „oxidált” nézetet.
Tehát, mi az erkölcsi? Klór, természetesen negatív. Vett valaki másnak a játék-elektron. Most negatív oxidációs állapotban van. Nátrium természetesen oxidált - amely elnyerte „savanyú” megjelenés. De a klór nem térhetnek - néhány játék nem több! Ami nem egy kép a kialakulása egy kémiai kötés egy tipikus redox reakció?
Már csak azt kell hozzátenni, hogy ilyen reakciók csökken oxidálószer. és oxidált - redukálószer. A mi történelem, klóratom - egy oxidálószer, és nátrium - redukálószer.