laboratóriumi munka
Célkitűzés: Tanulmányozni a fizikai és kémiai tulajdonságai a fenol.
Reagensek és eszközök: 2 n. HCl; HCl konc.; 2N. NH4 OH; 0,1. FeCl3; Br2 H2 O; AgNO3 - 0,2%; rezorcin - 1%; hidrokinon - 1%; pirogallol - 1%; A katekol - 1%; karbololajból víz, folyékony fenol.
állvány kémcsőbe; Szűrőpapír csíkokat (3x7 cm); pipettával.
Tapasztalat fenol 5.1 Oldhatóság vízben
Csőbe helyeztük 1 csepp folyékony fenolt adunk 1 csepp vizet, majd rázzuk. Forgassa zavaros folyadék - fenolt a-vízben emulzió. A teljes oldódás fenol vizet adunk cseppenként a víz, rázza az injekciós üveg minden egyes alkalommal. Határozzuk vízoldhatósága cseppfolyósított fenollal, fenol ismeri a jellegzetes szagú. A kapott fenolos visszatartott víz a további kísérletekben.
A tapasztalat 5.2 Színreakció a fenolos csoportot
Pipettázzunk elhelyezett 3 csepp átlátszó fenolos vizet egy másik csőbe, és 1 csepp 0,1 n. FeCl3. Mi van, ha ez bekövetkezik? 1 csepp 2n.HCl. Akár színező eltűnik? Egy másik kémcsőben bemérünk 1 csepp víz és átlátható karbololajból hozzácsepegtetik 2n.NH4 3OH, majd 3 csepp telített vizes brómos vizet, majd néhány másodperc után egy fehér papírra háttérkép kék festődés látható.
5.3 A tapasztalat Oktatási tribrómfenol
Helyeztünk egy kémcsőbe 3 csepp brómot adunk hozzá vizet, és 1 csepp fenol átlátszó víz. Brómoldatot vízzel színtelenítjük és kiválasztódik fehér csapadékot tribrómfenol. Így a reakció egyenletet. Összehasonlítás az arány a víz brómot benzol és fenol. Mi az oka, hogy a különböző reaktivitás?
Tapasztalat 5.4 Proof savas fenol
A maradékhoz vizet adunk, fenolos további 1 csepp fenol és rázzuk, az újonnan kapott zavaros emulziót fenolt adunk 1 csepp 2 n összesen. Nátrium-hidroxiddal. Ebben a pillanatban egy tiszta oldat. Hogyan magyarázza ezt? Ehhez a tiszta oldathoz hozzáadunk 1 kaplyuHCl. Hogyan tudjuk megmagyarázni a megjelenése üledék? Mert a reakciókat.
A tapasztalat 5.5 Színreakció fenolok vas-kloriddal
A négy fiolákat, rendre, 3 csepp 1% -os oldatok A katekol, rezorcinol, a hidrokinon és a pirogallol. Ahhoz, hogy minden egyes cső 1 csepp 0,1 n. FeCl3 oldatot. Mi van, ha ez bekövetkezik? Írja le észrevételeit. Az egyértelműség kedvéért, a szűrőpapírcsíkra (3x7) letétbe 2 csepp katechol és pirogallol megoldásokat. Amikor rastekutsya csepp a közepén minden helyszínen put 1 csepp rastvoraFeCl3. Csatolása kapott minták kromatogramjain az ő üzemi naplót.
Kérdések az ellenőrzési
1. Szerkezet és izoméria fenol és homológjai.
2. interferenciája hidroxil- és benzolgyűrű a fenol molekulában.
3. fenol és az aromás gyűrű és a hidroxilcsoport.
4. A különbség a szerkezetét és kémiai tulajdonságait fenolok és aromás alkoholok.
5. Ipari eljárások előállítására fenol.
Gyakorlatok: „fenolok”
1. Kijelző fenolok általános képletű C8 H10 O készítmény benzolgyűrűvel rendelkező, egy alkilcsoportot, és elnevezni őket.
2. Mely vegyületeket a lúgos hidrolízisével a következő vegyületek: a klór-benzol, o-nitrochlorobenzene, 2,4,6-trinitrohlorbenzola? Bármely vegyület esetében a hidrolízis reakció több, és miért?
3. Írja vevőáramkör o-krezol és 2,6-dinitro-fenol benzolból. Hasonlítsuk össze a hatás a metilcsoport és nitrocsoport a savas tulajdonságai fenolok.
4. Write p-krezol, hogy a reakciót nátrium-hidroxiddal, klorid etánsav, brómos vizet.
5. Hogyan lehet benzol, anizol?
6. Írja rendszer kialakulását m-bróm-fenolt benzolszulfonsav.
7. A get p-toluol hidroximetilfenolt és írni az utolsó reakció PCI 5 iNaOH.
8. benzol kap katechin, rezorcin, hidrokinon, guaiakol.
9. A p-amino-fenol és p-hidroxi-metil írási reakció -ecetsav-anhidrid.
10. Írja be a reakciókat, amelyek az interakció:
a) nátrium-fenolátot a hloretanom;
b) klór-benzol nátrium-izopropoxid.
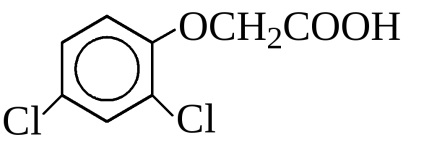
11. Javasolj konverziós áramkör benzol 2,4-diklór-fenoxiecetsav
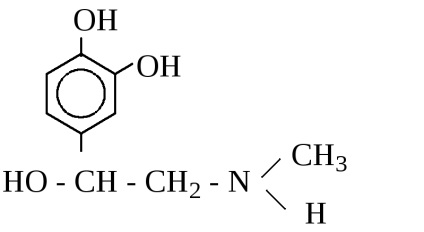
12. olvasó áramkörtől kölcsönhatás adrenalin -ecetsav-anhidrid
13. Töltsük fel a következő séma egymást követő átalakulások:
14. Töltse az alábbi transzformációs rendszer: