Komplex vegyületek - studopediya
Között a biológiailag aktív anyagok a szervezetben a fémionok különleges helyet foglalnak el. Tehát biokationy a legérzékenyebb „kémiai pont” a test. Ezek a tápanyagok élet a szervezetben, elsősorban a formájában a vizes oldatai sóik és komplex (koordináció) vegyületek.
Komplex vegyületek azok a vegyületek, a kristályrácsban, amelyek összetett részecskék csomópontok (komplex ionok), amely egy központi atom vagy ion és a környező semleges molekulák vagy ionok. Komplex ionok nem pusztította el őket egy elhaladó oldat vagy olvadék.
A szerkezet a komplex vegyületek már ismertetésre került a koordinációs elmélete Werner A. (1893). Szerint a koordinációs elmélet Werner komplex vegyületeket jellemzi egy adott térbeli elrendezése részecskék, az azokat alkotó molekulák. Például: K + | - CN - | K +
A fenti koordinációs képlet azt mutatja, hogy az egyik ion foglalja el a központi helyet. Ezt nevezik az atom vagy ion kelátképző. A legtöbb komplexképző szerek a pozitívan töltött fémionok, a legtöbb fém szekunder alcsoportok (D- és F-elemek), sokkal kevésbé - a semleges fém atomok (Fe, Ni) és a negatív töltésű atomok a nem-fémek (N -3 O -2 S ..). Jellemző komplexképző hatóanyagok fémek, például Fe, Cu, Ag, Au, Hg, Co, Cr, Mn, Cd, Ni, Pt, és mások. D- és F-elemek. Közel a komplexképző szer egy bizonyos sorrendben elhelyezett poláros molekulák vagy ionok az ellenkező megjelölés, és néha mindkettő, ezek az úgynevezett ligandumok (ligandok), hogy a „kapcsolódó” eszközök. ligandumok elengedhetetlenek:
a) semleges molekulák dipólus karakter: H2 O, NH3. CO, NO, C2 H4.
b) ionok: H -. O -2. OH -. Cl -. J -. Br -. CN -. HCO3 -. valamint egy bioligand makromolekulák aminosavaknak és ezek származékai, a peptidek, fehérjék, enzimek, hormonok, nukleinsavak és ezek fragmensei.
És komplexképző ligandumok képezik belső gömb (jelzi zárójelben), valamint az ionok nem szerepelnek a belső szférában, a külső gömb formájú. Belső Szféra gyakran szögletes zárójelek között. A díjat a komplex ion egyenlő az algebrai összege díjak és komplexképző ligandumok. A ligandumok száma, amelyek közvetlen közelében található, hogy a központi ion, az ion nazyvayutsyakoordinatsionnym számát (cn). Gyakran két koordinációs szám fordul elő, 4., 6. Általában a koordinációs szám kétszerese a díjat komplexképző ion kivétel Fe 2+. amelyekre cn 6 egyenlő Pt 4+ - 6.
Ha a ligandumok kapcsolódnak egy egyszeres kötés, és komplexképző foglalnak el koordinációs helyet a belső terén a komplex, az ilyen ligandumokat említett monodentantnymi (OH -. Cl -. J -. Br -. CN), két -bidentantnymi (CO3 2- 2- C2 O4). - birtokukban 2 koordinációs helyeket. Néhány ligandumok kapcsolódnak a központi ion és számos koordinációs kötést. Így többek között a komplex szerves vegyületek azok, akik szerepet játszhatnak a három, tetra - és több - hívják őket többfogú. Többfogú szerves ligandumok, zárt két vagy több koordinációs kötést képezhetnek gyűrűs komplexek.
Molekula-komplexek különböző, jól meghatározott geometriai szerkezetét. Például, két ligandum gyakran közelében található a fémion úgy, hogy a központi ion és a ligandum 2 kollineárisak. Három ligandumok találhatók a sarkokban egy háromszög, négy - a sarkában egy négyzet vagy tetraéder (Tetrahedron), hat - a sarkokban az oktaéder (oktaéder), nyolc - a sarkokban a kocka. Ha a ligandumok nem azonos, akkor a geometriai forma nem lehet teljesen helyes (torzított), de ennek ellenére, a ligandumok rögzített egyes pontjain a tér körül a központi ion.
Komplex vegyületek szerint osztályozzák a töltés a komplex ion, és a ligandum típusa. Szerint a felelős a komplex ion kationos komplexek (a komplex egy pozitív töltés), anionos (negatív töltésű komplex), semleges (komplex nulla töltés).
By típusú ligandum komplexek: acidocomplexes - ligandumok-maradékok (Cl - J - Br - CN - HCO3 - CO3 2- C2 O4 2 -......); hidroxi komplexek (OH -); aqua komplexeket (H2 O); amino komplexek (NH3); összekeverve, ha a komplex tartalmaz többféle ligandum.
Ezért, meg kell tudni, hogy a helyes írásmódját egy komplex általános képletű vegyület: töltés (oxidáció) komplexképző szert; a felelős a ligandumok; A koordinációs száma komplexképző szer; külső gömb ionok.
Írásakor képletek komplex ion komplexképző első szimbólum jelzi, akkor semleges ligandumok jelzett sorrendben H2 O, NH3. Miután semleges ligandumok kövesse anionos ligandumok. Anionos ligandumok sorrendben vannak felsorolva: N -. On -2. OH -. egyszerű anionok, anionok szervetlen komplex savak, vagy szerves savaknak.
Komplex képletű vegyületek szigorúan jobbról balra, rendet tartani a képlet ligandok helyét. A neveket a komplex vegyületek úgynevezett első anion a alanyeset, majd kation birtokos.
I. Ha a vegyület szerepel a komplex kation. Az első az úgynevezett ligandumok sorrendben helyen, a komplex, majd a komplexképző reagens neve (orosz elem neve). A zárójelben római számokkal jelzik a mértékét komplexképző oxidáció. Semleges molekulák működnek ligandumok, megvan a közös név, kivéve ammónia - amin, a víz - a víz, CO - karbonil, NO - nitrozil. A negatív töltésű ligandumok úgynevezett végződő „o”. Például, az N - - hidrid-, O -2 - oxo-, OH - - hidroxo, F - - fluor, Cl - - klór, S -2 - tio, CN - - ciano, SO4 -2 - szulfato, CH3COO- - - acetáto , CNS - - tiocianátocsoport, C2 O4 -2 - oxaláto. Ha több ligandumok, az eredetileg hívott ion külső gömb, majd ligandumok görög számokkai: - 2-di, 3-három, stb
Például: a neve a komplex kationok
[Co H2 O (NH3) 5] CI 3 - pentaamminakvakobalta-klorid (III)
[Pt (NH3) 5 Cl] CI 3 - hloropentaamminplatiny-klorid (IV)
[Pt H2 O (NH3) 2 OH] NO3 - gidroksodiamminakvaplatiny nitrátot (II)
II. Ha a vegyületet tartalmazza komplex anion. Az első az úgynevezett ligandumok a sorrendben a fent felsorolt. Továbbiakban komplexképző szer alkalmazásával gyökere a latin neve, hozzá egy szótag - „atomi”, ami után a római számokkal zárójelben fokú komplexképző oxidáció. Legalábbis a külső gömb nevezzük kation a birtokos eset. Például:
K [Ag (CN) 2] - ditsianoargentat (I) Kálium
K2 [Cu Ci-4] - tetrahlorokuprat (II) kálium-
K3 [Fe (CN) 6] - ferrát (III) kálium-
Név semleges komplexek alkotják a nevét a ligandumok és az orosz komplexképző reagens neve az alanyeset. Ebben az esetben, a vegyérték a komplexképző hatóanyag nincs megadva. Például: [Co (NH3) 3 Cl3] - trihlorotriamminkobalt.
[Pt (NH3) 2 Ci-4] - tetrahlorodiamminplatina.
A belső és a külső gömböt molekulák a komplex vegyületek kapcsolódó ionos kötésekkel. És komplexképző ligandum kapcsolódik kovalens kötéssel a donor-akceptor mechanizmus: ligandumok donorként egy elektronpár, és a komplexképző szer - a szerepe az akceptor. pályák a szabad elektronpár, amely egy ligand.
A disszociációs a komplex vegyületek két stádiumban megy végbe. Elsődleges disszociációja a komplex vegyületek azon ionizációs típusú erős elektrolitok, és egyenletesen áramlik: [Ag (NH3) 2] Cl → [Ag (NH3) 2] + + Cl -
Komplexáló ligandumok kötött erősebb kötés, és a disszociációs a komplex ion történik kisebb mértékben. Ez a fajta disszociáció az úgynevezett másodlagos.
Az intézkedés a komplex stabilitása ion az instabilitása állandó, és jelöljük Kn.
Minél kisebb az állandó instabilitás, annál stabilabb a komplex.
Komplex vegyületek fontos szerepet játszanak az életfolyamatok a növények és állatok. komplex vegyületek végre a különböző funkciók a szervezetben az állatok és növények: a felhalmozási és a mozgás a különböző anyagok és az energia; a kialakulását és hasítása kémiai kötések; részvétel a folyamatokban a légzés, fotoszintézis, a biológiai oxidáció és enzimes katalízis. Az ilyen biológiailag fontos anyagok, mint a hemoglobin, a klorofill, tsiankobolamin vannak kelát, a kelát vegyületek. Ebben a négy koordinációs helyek által elfoglalt egy részecske, úgynevezett porfin, komplexképző szer hemoglobin - Fe +2. és a klorofill - Mg 2. B12-vitamin - Co +3.
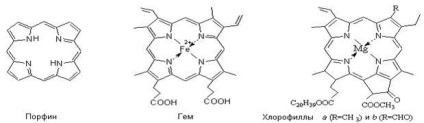
Porfirin vaskomplex sík szerkezettel, ahol a vas-ion csatlakozik koordinációs kötést 4 pirrolgyűrűhöz 4, 5 vannak kommunikációs csatlakozási globin fehérje, de a hatodik koordinációs szférában szabadon. Ez a hely, és azon oxigén molekula hemoglobin által szállított, a légzési folyamat.
Újabban megállapították, hogy komplexek platina és palládium van gátló hatása a malignus tumorok és sikeresen használhatók terápiás célokra, kelátképző (kelát) vegyületeket alkalmazunk a sók feloldva vesekő és csökkentve a víz keménységét jelenléte miatt a kalcium-ionok és magnézium. Ismert nagy baktériumölő hatásának néhány komplex vegyületek ezüst. Trilon B (EDTA) komplexet képezhetnek sok fémet, beleértve Ca +2. Ez lehetővé teszi annak alkalmazását járó betegségek túlzott mértékű lerakódása kalciumsók a szervezetben.