Standardpotenciál
A számítási módszere változás, vagy az abszolút értéke az elektród potenciál ugrik, amíg naydeno.Odnako EMF álló lánc két vagy több elektród, lásd az algebrai összege minden ugrások határfelületi potenciálok. A legegyszerűbb esetben, ez egyenlő a különbség a két ugrik az elektród potenciál, azaz Ez az intézkedés a relatív értékeket. A nagysága az egyes elektród potenciál ugrások lehet elfogadni a nulla pont a skála feltételes elektródpotenciálok. Nemzetközi megállapodás létrehozta a potenciális körét, ahol a feszültségesés a standard hidrogén elektród minden hőmérsékleten nullával egyenlő.
Standard hidrogén elektród áll platina bevonatú platina érintkező az oldatot, a hidrogén-ion aktivitása, amely (H2 SO4), és mossuk a hidrogéngáz áramot gáz hidrogén nyomáson.
elektród folyamat
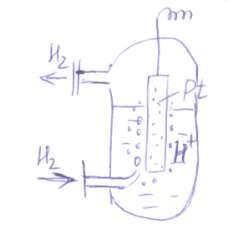
3 magában foglalja a következő lépéseket:
1. adszorpciója molekuláris hidrogén platina;
2. disszociációja az adszorbeált molekulák az adott atomon gyorsított katalitikusan platina;
3. Az ionizációs atomos hidrogén és annak átmenetet az oldatba
A harmadik szakasz határozza meg a megjelenését az elektróda potenciál csepp, és ezért az úgynevezett potenciális meghatározó. Így egy egyensúly jön létre a hidrogén-ionok az oldatban és a hidrogén gáz.
A hidrogén-elektród van írva a következő:
Az elektróda potenciálja a hidrogén-elektród van írva a Nernst-egyenlet:
Ahogy a hidrogén parciális nyomása megegyezik az egység = 1, ez a kifejezés egyszerűsödik
standard hidrogén elektród potenciál a hidrogén-ion aktivitás = 1, olyan körülmények között, ahol a hidrogéngáz nyomása megegyezik az egység = 1, és a hőmérséklet 289K, kapott nulla (0).
A elektród potenciálját ugrás tetszőleges léptékű hidrogén elektród úgynevezett elektródpotenciál és jelentette. Ez megegyezik az EMF az elektrokémiai cella, amely egy standard hidrogén elektród és a. Rögzítése az ilyen elementavsegda kezdődik a hidrogén-elektród, azaz a úgy vélik, hogy a bal oldalon.
Potenciálja mérőelektródaként
Ahhoz, hogy meghatározzuk a elektródpotenciál összegyűjtjük galvánelem, amely egy elektród, a potenciális, amelyek mi érdekli, és a standard hidrogén elektród, majd mérjük a EMF ennek az elemnek.
Standard hidrogén elektród, amelynek lehetséges vesszük nullával egyenlő, és amely mindig maradt képest a másik elektród, van írva a következő:
Mi határozza meg a lehetséges cinkelektródára. Cink elektród van írva, mint:
A potenciális ezt elektróda által meghatározott elektromotoros erő sejt.
A tapasztalat azt mutatja, hogy ha az elem cink oxidálódik: Így lehetséges az cink elektoroda kell rendelni negatív előjelű. Abszolút értéke a cink elektróda:
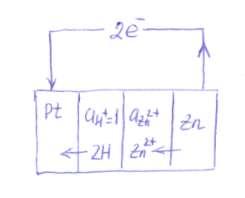
Mivel a töltés több negatív cink platina töltés, elektron fog elmozdulni a cink, a platina, azaz jobbról balra. Ugyanabba az irányba, és ez jellemző a negatív elektród egy pár egy standard hidrogén elektród, és a kationok át releváns elemet megoldásokat.
Ellentétben a réz elektróda a cink elektróda pozitív potenciál, a megfelelő EMF pozitív elem:
Itt a rézelektród spontán redukciós reakciót:
EMF Ezen elem egyenlő lesz a potenciális a réz elektróda.
Ha az aktív ionok réz és a cink, amelyek egyenlő egységét, a megfelelő EMF elem határozza meg szabványos potenciálok réz és cink elektródákat.
-Standard elektród potenciálja a cink elektród.
Standardpotenciál alkotnak egy sorban, amely hivatkozva rendszerek fém - fémionok a vizes oldatban megfelel a helyét a fém a kémiai aktivitást, azaz feszültség tartomány: