Móltömeg acetilén (C2H2), és példák a általános képletű
A moláris tömege acetilén
Acetilén - egy komplex anyag szerves természetű. Progenitor homológ sor alkinek (telítetlen szénhidrogéneket egy hármas kötést).
A szerkezet a acetilén molekula ábrán látható. 1. Normál körülmények között színtelen gáz, könnyebb, mint a levegő. Szagtalan. Gyengén oldódik vízben, de jól atsetone.Vzryvoopasen.
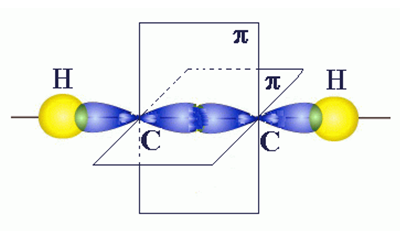
Ábra. 1. A szerkezet a acetilén molekula.
Molekuláris képlet acetilén - C2 H2. Mint ismeretes, a molekulatömege a molekula az összege a relatív atomi tömegek a atom alkotja a molekula (relatív atomtömeg értékeket vett Mendeleev Periódusos Táblázat egész számra kerekítve).
Úr (C2 H2) = 2 × 12 × 2 + 1 = 24 + 2 = 26.
Móltömeg (M) - a súlya 1 mol hatóanyagra vonatkoztatva. Könnyen azt mutatják, hogy a számértékek a moláris tömege, és a relatív molekulatömeg úr egyenlő, de az első érték az alábbi méretekkel rendelkezik [M] = g / mol, és egy második dimenzió:
Ez azt jelenti, hogy a molekulatömeg-acetilén 26 g / mol.
Példák problémák megoldása
Tedd képletű kálium, kén és oxigén, ha a tömegarányai elemek benne: ω (K) = 30,75%, ω (S) = 25,21%, ω (O) = 44,04%.
Tömeghányada X elem a molekulában HX készítmény kiszámítani a következő képlet:
ω (X) = n × Ar (X) / M (HX) × 100%.
Jelöljük a mólszáma tartozó elemek a csatlakozások az „x” (kálium) „y” (kén), «z» (oxigén). Ezután a mólarány a következő lesz (az értékek a relatív atomi tömegeket vett Mendeleev periódusos, egész számra kerekítve):
x: y: z = ω (K) / Ar (K). ω (S) / Ar (S). ω (O) / Ar (O);
x: y: z = 30,75 / 39. 25,21 / 32: 44,04 / 16;
x: y: z = 0,78. 0,78: 2,75 = 1. 1. 3.
Ezért általános képletű kálium, kén és oxigén lesz a formában KSO3.
Tedd képletű nátrium-vegyületek, a szén és az oxigén, amikor a tömeg frakciók elemek benne: ω (Na) = 43,4%, ω (C) = 11,3%, ω (O) = 45,3%.
Tömeghányada X elem a molekulában HX készítmény kiszámítani a következő képlet:
ω (X) = n × Ar (X) / M (HX) × 100%.
Jelöljük a mólszáma tartozó elemek a csatlakozások az „x” (nátrium) „y” (szén), «z» (oxigén). Ezután a mólarány a következő lesz (az értékek a relatív atomi tömegeket vett Mendeleev periódusos, egész számra kerekítve):
x: y: z = ω (Na) / Ar (Na). ω (C) / Ar (C). ω (O) / Ar (O);
x: y: z = 43,4 / 23. 11.3 / 12: 45,3 / 16;
x: y: z = 1,9. 0,94: 2,83 = 2. 1. 3.
Ezért általános képletű nátrium-vegyület, a szén, és az oxigén lesz a formában Na 2CO 3. Ez a nátrium-karbonát.