Molekuláris erők - studopediya 1
Sok tapasztalati tények arra engednek következtetni, hogy a molekulák közötti egy anyag bármely Halmazában jár mind az erők a vonzás és taszítás erő-Bani. Például, a képessége, szilárd kifejtő rezisztencia-stretching Lenie jelenlétét jelzi a vonzó- molekulák közötti; létezik a taszító erők magyarázza a kis összenyomhatóság szilárd anyagok és folyadékok, valamint erősen tömörített ha-hívást. Nagyon fontos, hogy ezek az erők cselekedni egyszerre. Ellenkező esetben, a test nem lenne stabil: hogy képező ő mo-molekulák szétrepülnek ellentétes irányban (ha csak taszító erők), létrehozására ultra-kis sűrűségű anyag, vagy „fúziós-palis” lenne szupersűrű aggregátumok (ha már csak vonzó-).
A számítás a kölcsönhatás erők a molekulák közötti, és megvilágította a természet e erők csak akkor lehetséges keretein belül kvantummechanika. Azonban ha acteristic, kvalitatív formában a molekuláris erők állíthatjuk elő Ost-Vayas belül leggyakoribb klasszikus fogalmak.
Az erők közötti molekulák a természetben Xia erők az elektromágneses eredetű. A molekula olyan pozitív töltésű atommag alkotó atomok a molekula, és a negatív töltésű elektronhéjakat atomok. Ezért, ha a molekuláris kölcsönhatások ugyanakkor, mint az erők vonzási ellentétben díjak és erők taszítása hasonlók. Mindkettő közötti távolság a molekulák-gyorsan csökken. Azonban, a csökkenés a taszító erők gyorsabbnak kell lennie, mint a gravitációs erő, ami egy taszító erő lesz előre rendelkeznek a kis távolság a molekulák közötti és a vonzó- - nagyobb távolságokon. Az utolsó állítás következik szükségességét létezésének stabil egyensúlyi Interact-nek molekulák. Tény, hogy tegyük fel, hogy a két kölcsönható molekulák egyensúlyi állapotban vannak, azaz, összege ható erők minden molekula nullával egyenlő. 1. ábra, valamint ábrázolja a két mól-Kula, található a parttól, hogy a taszító erő F1 ellensúlyozni az erők kölcsönös vonzás F2. Legyen a távolság molekulák között csökken (1b ábra). Ha a taszító erő gyorsabban növekszik, mint a vonzóerő, az F1 lesz F2. és molekulák kerülnek szorult vissza egyensúlyát. Ha a köztük lévő távolság nagyobb, mint az egyensúlyi edik (1. ábra, B), és az F1 kisebb lesz, mint az F2. A molekulák ismét keresik egyensúlyi helyzet.
Így ha bebizonyosodik, hogy a szempontjából a stabilitás a taszító erők gyorsan csökken a távolság, mint a gravitációs erő. A távolságok molekulák között, sokkal nagyobb átmérőjű (1. ábra, g) gyakorlatilag nincs interakció molekula-léteznek, mert az elektronok kering a sejtmagok teljes egészében kompenzálja valaki díjak ezek a magok és a molekulák általában semlegesek. Amikor közeledik molekulák (1. ábra, d) fokozatosan nyilvánul köl-kölcsönható elektromos töltések sejtmagok és molekulák az elektron pályák. Ez annak köszönhető, hogy a vonzereje egy névleges díjat a szemközti és taszítás. Ennek eredményeként, enyhe deformáció lép fel (a polarizációja) a két kölcsönható molekulák, mint a hagyományosan hosszú Zano ábrán 1 d. Ennek következtében a molekulák keletkeznek gravitáció. A további közeledése a polarizáció a molekulák és az ólom-tier vonzóerők növekedni fog. Ha a molekulák jönnek közelebb olyan mértékben, hogy azok elektron felhők kezdenek észrevehetően hatol egymásba, az elektronok és a sejtmag különböző molekulák gyorsan-felengedett bólint olyan erővel, amely gyorsan növekszik csökkenő közötti távolság molekulák. Ilyen távolságok fog dominálni az erők a taszítás (1. ábra, e).
Abszolút értéke a kölcsönhatás erő lényegében attól függ, hogy az adott molekuláris szerkezetet. Ezen túlmenően, a nem-gömb alakú molekulák elektromos kölcsönhatást erők függenek, nyilvánvalóan, nem csak a távolságot a molekulák, hanem a kölcsönös tájékozódás a molekulák. Ugyanakkor az általános jellegű kölcsönhatás erők a távolság ugyanaz: az uralkodó vonzó erők nagy távolságból és visszataszító-CIÓ alacsony.
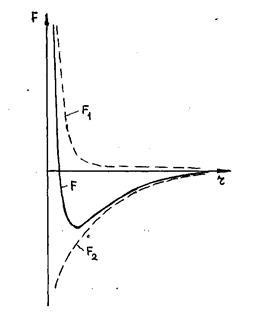
Az így kapott F funkció = F1 + F2 látható az ábra mutatja, a folytonos vonal. Amint látható, a távolságok r
A molekuláris fizika nem működnek az erők, és a potenciális energia-kormányzati kölcsönhatásokat. Ahhoz, hogy az átmenet erő a potenciális energia, tartjuk a munkát, amelyet az Eredő-al F erő, ha a távolság a molekulák a dr:
Ezt a munkát azáltal, hogy csökkenti a potenciális energia kölcsönhatása molekulák:
A kifejezést (B.11) és (B.12)
Integrálása egyenlet (B.13) szerinti r r a végtelenbe,
A potenciális energia nullának tekintjük egy végtelenül nagy távolság a molekulák, azaz . majd
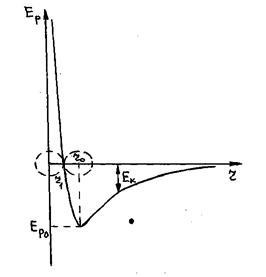
Az ábra azt mutatja, hogy amikor a mozgó molekula egy molekula 2-től a végtelenig, ami található a származási-feszültséget, a kölcsönhatás a potenciális energia csökken nullától ep0. Ebben része az elmozdulás, azaz a R = ∞, hogy r = r0. 1 hat a molekula a vonzóerő, ami növeli annak skoroct (kinetikus energia). A további közelítése molekulák (a részen, ahol R
Kapcsolódó cikkek