hidrogén-elektród
Standard hidrogén elektród - elektródát használunk, mint a referencia elektród különböző elektrokémiai mérések és a galvánelemek. A pH-elektróda (RE) egy lemez vagy drót fémből, valamint hidrogén-elnyelő gáz (általánosan használt platina vagy palládium), telített hidrogénnel (atmoszferikus nyomáson), és elmerül a vizes oldatban. tartalmazó hidrogén-ionok. A lehetséges a lemez függ [meghatározott] koncentrációjának H + ionok oldatban. Az elektróda az a standard, amelyhez az elektród potenciál számít meghatározott kémiai reakció. A hidrogén nyomás 1 atm. koncentrációja protonok oldatban 1 mol / l, és a hőmérséklet 298 K VE potenciál van beállítva, hogy 0 V Amikor a szerelvény az elektrokémiai cella által meghatározott elektródák RE és a reverzibilis reakció következik be a platina felületen:
azaz, az vagy hidrogén-visszanyerés, vagy annak oxidációs - ez függ a kapacitás a reakció előforduló az elektróda meghatározva. Mérésével az EMF az elektrokémiai elektród standard körülmények között (lásd. Felett) meghatározzuk a standardpotenciál által meghatározott kémiai reakció.
Számítóelemeket mérésére használunk a standard elektród potenciálja az elektrokémiai reakció, koncentrációjának mérésére (aktivitás) a hidrogén-ionok és bármely más ionok. VE alkalmazva is meghatároztuk az oldhatóságot, a termék, hogy meghatározzuk a sebességi állandókat az egyes elektrokémiai reakciók.
A legfontosabb követelmények a referencia elektróda:
1) Az elektróda kell működnie a hőmérséklet-tartományban.
2) A stabilitást.
3) Az az eredmények reprodukálhatósága.
4) összeegyeztethetőnek kell lennie a vizsgálat elolvad.
5) hiánya helyhez potenciálok.
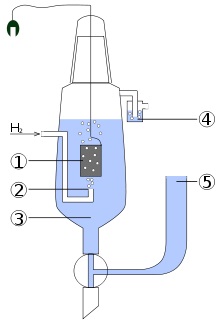
Reakcióvázlat standard hidrogén elektród:
- Platina elektród.
- A mellékelt hidrogéngáz.
- A sav (jellemzően HCI), ahol a koncentrációja H + = 1 mol / l.
- Vízzár, amely megakadályozza a behatolását légköri oxigén.
- Elektrolitikus híd (amely egy koncentrált KCl oldat), amely lehetővé teszi, hogy csatlakoztassa a második felében a cella.
Bonyolultsága ellenére művelet (szükség van egy állandó beáramlása hidrogéngáz) a hidrogén-elektród már régóta ismert.
- Hidrogén elektródák saját tervezés volt a központi eszköze működik SP L. Sorensen. amely megjelent eredményeként a modern elmélet pH-mérő (1909).
- Az első kísérletekben a gyomron belüli pH-metria pH-mérőt használunk. JF McClendon. egy referencia elektród, amelyben a hidrogén-elektród került be az összetétele a pH-szonda az emberi gyomorban (1915).