Eljárások oxigénnel depolarizációval
A folyamatok fém korróziós amelyben a katódos depolarizáció végezzük oldott oxigén az elektrolitban, úgynevezett folyamatok fémkorrózió oxigénnel depolarizációt. Oxigén depolarizáció - katódos redukciós reakciót (ionizáció) az oxigén. A oxigén depolarizáció, a leggyakoribb eljárás korrodálja fémek a légkörben (fém eszközök különféle növények, a különböző hűtési rendszerek) hüvelyébe folyami és tengeri hajók, csővezetékek és különböző más.
korróziós folyamatok oxigénnel depolarizációs fordulhat elő, ha a következő feltétel:
ahol: (4,53) - reverzibilis potenciálja az oxigén elektród ilyen körülmények között; () Mod - szabványos potenciálja az oxigén elektród 25 0 C-on (reverzibilis potenciálja az oxigén elektród, amikor nOH - = 1 és = 1 atm = 1.013 10 5 Pa.); - az oxigén parciális nyomása; nOH - - Activity hidroxil ionok. A semleges és lúgos oldatok ionizálásra O2 molekulák végbe, hogy a reakció: O2 + 2H2 O + 4e = 4OH-t -.
Az érték a reverzibilis potenciálját az oxigén elektród 25 o C-on különböző pH-értékek, és a táblázatban felsorolt. 4.2.
0,21 (a légkörben)
Reakcióvázlat katódos folyamat több, egymást követő szakaszból áll:
1) oldjuk légköri oxigén az elektrolit;
2) átvitele az oldott oxigén mennyisége az elektrolit a katód felületére természetes konvekcióval vagy keverés közben;
3) átadása oldott oxigén a diffúziója következtében fellépő O2 molekulák az ömlesztett a felszínre a katód;
4) Ionizációs oxigénmolekulák semleges és lúgos oldatokban:
savas oldatokban a következő reakcióegyenlet szerint:
5) semleges vagy lúgos oldatok - diffúzió és konvektív szállításával ionok OH - a katód felületét be a nagy részét az elektrolit, vagy a reakció, hogy egy oldható fém-hidroxid: Me n + + nOH - = Me (OH) n.
A legtöbb esetben, a korrózió oxigénnel depolarizációval leginkább gátolt katód eljárási lépések: nyugtató elektrolitok - oxigén diffúzióját; oxigént nagy sebességgel, hogy a korrodáló fém (erős keverés az elektrolit vagy a vékony film elektrolit a fém felületén) - ionizációs oxigén. Gyakran van egy arányban gátolja mindkét szakaszban.
Elektrokémiai polarizáció miatt a lassúsága a reakciók (4,53-4,54), amely hiányában a polarizáció kell történnie a katód potenciál egyenlő. Ez az úgynevezett oxigén túlfeszültséget ionizáció. Oxigén túlfeszültséget ionizációs függ a katódos áramsűrűség a katód anyagának, a hőmérséklet, stb
Alacsony sűrűség, katód áram (<10 -2 А/м 2 ) перенапряжение ионизации кислорода прямо пропорционально зависит от плотности тока (участок А на рис. 4.12):
ahol IK - állandó az anyagtól függően, és felületének állapotát a katód, a hőmérséklet, stb
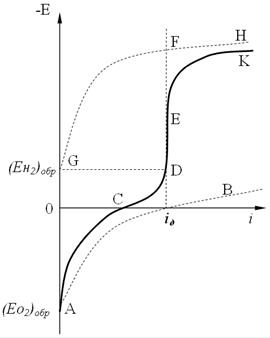
Ábra. 4.12. Katódos polarizációs görbe: AB - oxigén túlfeszültséget ionizáció; GH - a hidrogén túlfeszültség; CDEK - összesen katódos polarizációs görbét.
A magas áramsűrűség (> 10 -2 A / m 2), valamint egy lényegében az oxigén ellátó oxigénfogyasztás sebességének a katód túlfeszültség ionizációs logaritmikus függését az áramsűrűség:
ahol: a2 - függő konstans a katód anyag és felületi állapota, a hőmérséklet és más tényezők. Ez az a Ik = 1; b2 - állandó, annak a mechanizmus a ionizációs oxigén túlfeszültség egyenlő 2H, t / nF # 8729; 2303. 20 0 C-on, és n = 1, b2 = 0,117.
Polarizációs miatt lassúsága az oxigén diffúzióját a katód felületére nevezzük koncentráció ,; az értéke ez a polarizáció lehet kiszámítani a következő egyenlet szerint. (4,57)
ahol: n - az elektronok száma bevont katód ionizációs egy oxigén molekula; - az oxigén koncentráció a törzsoldatot; - az oxigén koncentráció a katód felületére.
Egy összefoglaló a koncentráció-polarizáció is ad egyenletet (4,49), figyelembe véve, hogy a teljes értéke az oxigén katód polarizációs:
ahol: Id - diffúziós áramsűrűség határértéknél, határozzuk meg kísérletileg kapott katódos polarizációs görbéket (ábra 4.12)., vagy számítással.
Amikor a fémek korróziója a elektrolitok a legtöbb esetben, egyes részei a fém felületén, hogy feloldódjon (anód) a másik folyamat előrehaladásával katód (katód) - heterogén korróziós mechanizmus. Egy ilyen szétválás felülete miatt a inhomogenitása a fémfelület (a jelenléte a különböző szemcseorientációs, szemcsehatár-fázisok Egy eltérő szerkezetű és összetételű, ficam klaszterek, zárványok és hasonlók).
Amikor az oxigén diffúzióját a katód (az általános esetben, a kocsi - visszavonása a reagensek a fémfelülethez) ND Tomashov kimutatták, hogy ha összegének kiszámításakor a diffundáló oxigén egyedi katód (ábra. 4.13), kell figyelembe venni mind a közvetlen és oldalirányú oxigén diffúzió útja. Ez annak köszönhető, hogy az a tény, hogy a diffúziós folyamat vesz részt nemcsak az elektrolitban BCDE hengertérfogat, hanem a többi térfogata az elektrolit. Ez a mennyiség megfelel egy első közelítésben, térfogata csonka kúp alakú FGDE (ábra. 4.13). Leegyszerűsítve katód telt kerek,
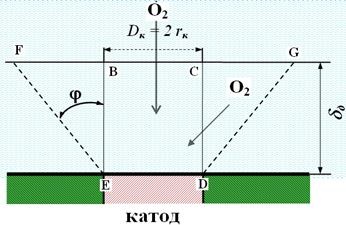
Ábra. 4.13. Reakcióvázlat oxigéndiffúziót egy kör alakú katód.
sugarú rk. Ezután attól függően, Fick törvény legfeljebb diffúziós áramsűrűség oxigén egyenlet érvényes:
ahol: - az oxigén koncentráció a törzsoldatot; D - a diffúziós együtthatót; # 948; d - a vastagsága a diffúziós réteg; # 966; = 51 0 50 / - közötti szög a kúp és a merőleges diffúzió.
Ha a méretei a katód sugár rc képest a diffúziós réteg vastagsága # 948; d meglehetősen nagy (makrokatody, ris.4.14 a), a második tag egyenletben (4,59) kicsi, és lehet elhanyagolni:
ha microcathodes (. ábra 4.14, b), akkor figyelmen kívül hagyják az első ciklus:
Ábra. 4.14. Reakcióvázlat diffúziós a makró (a) és microcathodes (b).
Mit lehet tekinteni makrokatoda vagy microcathodes ez függ a megengedhető hiba a közelítő számítást. Amikor egy hiba ne legyen nagyobb, mint 10%, és a vastagsága a diffúziós réteg # 948; d = 0,1 cm (közel az elektrolit) elfoglalhat méretek: az makrokatodov dk = 2rk ≥2 cm (DK - átmérőjű katód), hogy microcathodes dk ≤0,03 cm.
elősegíti a folyadék mozgását közlekedés anyag. A elmélete konvektív diffúzióját a diffúziós réteg vastagsága lehet becsülni, mint:
ahol v - kinematikus viszkozitását a folyadék, x - távolság a figyelembe vett pont az elektród felülete tekintetében a pont a folyadéksugár rámpa, vo - jet sebesség képest az elektróda.
Egyenletből (4,62) azt mutatja, hogy a diffúziós réteg vastagsága nem állandó a teljes felületen a rögzített elektróda, és ennek következtében korlátozzák diffúziós áramsűrűség függ A mérete és alakja az elektróda, és változik egy részét a másik felületre.
A korrózió oxigénnel depolarizáció semleges elektrolitok leginkább jellemző:
1) kialakítunk egy fém-film felületén, vagy morzsolható szekunder kicsapódása rosszul oldódó fém-hidroxidok;
2) ellenőrzik a diffúzióját a katódos folyamat (sűrűségben határérték közeli) egy viszonylag kis korrózió sebessége (viszonyítva a savat):
- nyugtató (nem kevert) elektrolitok,
- A föld alatti korrózió
- jelenlétében, mérsékelten oldódó fém felület korróziós termékek;
3) egy katódot diffúziós ellenőrzési folyamatban szennyeződések vagy strukturális komponensek, mint microcathodes kevés hatása van a korrózió sebességét, használata révén laterális diffúziós utak O2;
4) A kinetikus kontroll a katódos folyamat meghatározása, hogy mikor:
- Erős keverés közben az elektrolit (fém korróziós sebesség növekedésével),
- atmoszferikus korrózióval nedvesség által vékony film.
A diffúzió-kinetikus kontroll a katódos folyamat, a hatás a sebességét ionizációs a katód feszültség és a lassúsága a diffúziós összemérhető oxigént. Ez - a leggyakoribb esetben, fém korróziós oxigénnel depolarizációt. Ebben az esetben, a korrózió sebessége is érzékeny az oxigén diffúzióját körülmények között. Azonban a folyamat sebessége függ a jellegét és tartalmát szennyezések a katód, de kisebb mértékben, mint a tisztán kinetikus kontroll folyamatot.
Amikor egyenetlen hozzáférést az oxigén a vas felületén jelenik meg elektrokémiai cella eltérés levegőztetés - levegőztető elem (maró hatású eleme elektródákkal az azonos fém miatt bekövetkező nagyobb áramlási oxigén egy része a fém felületén).
Képlet (4,53), hogy a rész a magasabb koncentrációjú O2 lesz nagyobb potenciállal és működnek, mint a katód, a kisebb koncentrációjú - anódként. Ez a potenciális különbség elég nagy, és okozhat jelentős korróziós sebessége az anód. Példák a levegőztetés elem az az acél korrózióját cső a talajban különböző O2 áteresztőképesség (homok - agyag) (ábra 4.15.), Vagy korrózió acélszerkezetek a vízvonal.
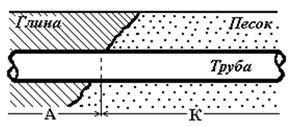
Ábra. 4.15. Előfordulás levegőztetés galvanikus pár átadásával a acélcső keresztül részei föld különböző légáteresztő.