Szerves savak és szervetlen
Már tudom, egy csomó bizonyos savak, mint egy olyan összetett anyagok.
Savak úgynevezett komplex típusú vegyületeket, amelyek a hidrogén atomok képesek szubsztituált fém, és egy savas maradékot.
Tekintettel az elektrolitos disszociáció elméletének a savak közé tartozik elektrolitok alkotó kationok upon disszociációja csak egy típusú - a hidratált hidrogén-ionok.
Az elmélet az elektrolitos disszociáció magyarázza a sav-bázis tulajdonságaiban vizes oldatainak elektrolitok jelenlétében feleslegben ezen ionok.
Ezzel együtt ismert reakciókban, amelyekben anyagok kölcsönhatásba, mint egy sav és egy bázis távollétében ezek a hidrogén-ionok és a hidroxid-ionok. Emlékezzünk, például a kialakulását ammónium-klorid reakciójával hidrogén-klorid és a gáz alakú ammóniát. ismert meg, mint a füst tűz nélkül.
1923-ban volt Protolytic elmélete savak és bázisok-Laur Johannes Nicolaus Bronsted és amely bővült fogalmakat a savak és bázisok, megmagyarázni a viselkedését anyagok vizes és nem-vizes (alkohol, éter, ammiachiyh) megoldásokat. Az elmélet szerint a sav - olyan molekulák vagy ionok, amelyek a reakcióban a hidrogén kationok H + donorok, amely adott nekik.
Ennek megfelelően csavarás - olyan molekulák vagy ionok, hogy prini mayutsya kationok H +, azaz ezek H + akceptorok.
A szempontból az elmélet elektrolit bomlási a ionok (I) és hidrolízissel a-anion (2) kezelik, amely sav-bázis kölcsönhatás elektrolitok és a víz.
Az (1) reakcióban H20 viselkedik, mint egy bázis - hozzáad egy proton (H +), és a oxónium-ion formái a donor-akceptor mechanizmus.
Most, hogy már ismeri a szélesebb véve irnrodu sav-bázis tulajdonságainak kémiai vegyületek, általánossá információt pentánsav osztályba, úgy a osztályozását és tulajdonságait szervetlen és szerves savakkal (lapon. 17).
tulajdonságai savak
Savanyú íz, hatása a mutatók, elektromos vezetőképesség, interakció fémekkel, alap- és amfoter oxidok, bázisok és sók, észterek képzése alkoholokkal - ezek a tulajdonságok megegyeznek a szervetlen és szerves savak.
1. A savas vizet, disszociál hidrogén kationok és anionok a savas maradékok, mint például:

Savas oldatokat változtatni a színét mutató: lakmusz - piros, narancs metil - rózsaszín fenolftalein nem változik.
2. megoldások savak reagálnak fémekkel. álló elektrokémiai feszültség sorozat maradt hidrogén, bizonyos feltételek mellett, a legfontosabb az, amely a kialakulását a reakció egy oldható sót.
3. a szervetlen és szerves savakkal kölcsönhatásba az alap és az amfoter oxidok, feltéve, hogy az oldható só képződik.
4. Mindkét savak reagálnak bázisokkal. A polibázikus savak képezhetők, mint az átlagos, és a savaddíciós sók (ebben semlegesítési reakció)
5. A reakció a sav és a só csak az esetben, ha egy csapadék, vagy egy gáz.
6. az észterek nemcsak a szerves sav szerint az általános egyenlet.
Egy hasonló reakciót ushetiem két vagy három hidroxil-csoport a cellulóz és annak nitrálási eredményez komplex zfirov: Li- és trinitrotsellyulozy - nagyon szükséges anyagok előállításához füstmentes lőpor.
Azonban, az egyes tagok az ásványi és szerves savakkal, valamint speciális tulajdonságokkal.
Ecetsav SN3SO0N más karbonsav tartalmaz egy szénhidrogén-csoport egy molekulában. Lehet halogén szubsztitúciós reakciót a hidrogén:
in-molekula hatása alatt a halogénatomok disszociációs foka jelentősen megnő. Például, hloruksus NJ-sav csaknem 100-szor erősebb, mint ecetsav (miért?).
Hangyasav HCOOH. in otlmchie ecetsav, azt a molekulában a szénhidrogéncsoport. Ehelyett tartalmaz hidrogénatom, és így olyan anyag, azzal a kettős funkció - és aldehid. Eltérően más karbonsavak, a reakciót ad „ezüst tükör”. A kapott szénsav N2S03 bomlik víz és a szén-dioxid.
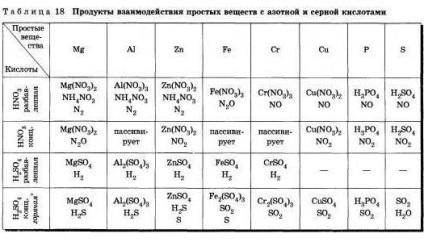
1. Mivel a savas jellegű befolyásolja a mértékét elektroliticheskoydissotsiatsii? Vegyük példaként a jelen befolyás: a) salétromsavat és nitrogén-savak, b) hipoklórsavoldó HClO és perklór NSl04. d) kénessav és kénsav. Készíts egy általános következtetést.
2. Tekintsük a interferenciát tartalmaz molekulánként Propp PNS sav-CH3-CH2-COOH, a terv szerint: a) a hatás a karboxil-csoport; b) a befolyása a karboxil-csoport; c) a befolyása karbonnla gidrokenl; g) a befolyása az hidroxilcsoport a karbonil.
3. Helyezze hlorpronzvodnye ecetsav növelése érdekében az erejüket. Indokolja válaszát.
4. Pochet salétromsav és kénsav (konc.) Sav viselkednek reakciókhoz eltérő fémekkel, például a sósavval?
8. A 730 g 12% hidrogén-kloridot feloldottunk 33.b l hidrogén-kloridot. Find hloropodoroda tömeghányada a kapott oldatban.
A válasz: 18.14%.
9. 820 g 0,5% -os vizes kénsav-oldatot feloldunk több 11.2l kén-dioxid. Mi volt a súlya frakció a sav az oldatban?
Válasz: 5,29%.
Ha javításokat és javaslatokat a leckét, kérjük lépjen kapcsolatba velünk.
Ha azt szeretnénk, hogy a többi beállítást és javaslatokat órák, nézd meg itt - Oktatási fórum.