Aggregációs állapotok az anyagban
Mint már említettük, a molekulát jellemző egyik legfontosabb paraméter az EP0 kölcsönhatásának minimális potenciálja. A molekulák között ható vonzáserő általában hajlamosítja az anyagot, azaz hogy molekuláit közelítse az r0 távolsághoz (3. ábra), amikor az interakció potenciális energiája minimális és egyenlő az EP0-val. de ezt a megközelítést akadályozza a molekulák kaotikus termikus mozgása. E mozgás intenzitását a molekula átlagos kinetikus energiája határozza meg, amely a kT sorrendje. ahol k a Boltzmann konstans. Egy anyag összesített állapota lényegében az EP0 és a kT értékek arányától függ.
Tegyük fel, hogy a vizsgált molekulák rendszerének hőmérséklete olyan magas, hogy kT >> EP0. Ebben az esetben az intenzív kaotikus hõmozgás meggátolja a vonzó erõket a molekulák összekapcsolására több olyan részecskék aggregátumával, amelyek r0 távolsággal konvergáltak. ütközéskor a molekulák nagy kinetikus energiája könnyen megtörheti ezeket az aggregátumokat alkotó molekulákká, és így a stabil aggregátumok képződésének valószínűsége önkényesen kicsi lesz. Ilyen körülmények között a vizsgált molekulák nyilvánvalóan gázállapotúak.
Ha a részecske-rendszer hőmérséklete nagyon alacsony, azaz kT < Végül a részecske-rendszer hőmérsékletén a kT ≈ EP0 közelítő egyenlőség alapján határozható meg. kinetikus energia hő Vågå molekuláris mozgását, amelynek értéke megközelítőleg egyenlő a potenciális vonzás energia-sósav nem tudja mozgatni a molekula a távolba beállított lényegesen magasabb, mint az R0. Ilyen körülmények között az anyag folyékony aggregátum állapotban lesz. Így az anyag hőmérsékletétől és az EP0 nagyságától függően. amely az alkotó molekulák egy adott csoportjához tartozik, gáznemű, szilárd vagy folyékony állapotban lesz. Ebben az esetben az egyik állapotból a másikra történő átmenet hőmérsékletét az adott anyag (fajta molekulák) jellemző EP0 száma határozza meg. Ismeretes, hogy inert gázokban (hélium, neon, argon stb.) Az EP0 értéke viszonylag kicsi. Ezért széles hőmérséklet-tartományban gázállapotúak és nagyon alacsony hőmérsékleten, az abszolút nulla érték közelében haladnak a folyadékba. EP0 fémek esetén. éppen ellenkezőleg, általában nagy. Ezért a megfelelően magas hőmérsékleteken a fémek szilárd állapotban vannak. Összefoglalva elmondhatjuk, hogy ha az anyag van Ennek a résznek a megkötésekor jegyezzük meg, hogy milyen mozgások egy olyan molekuláris anyag, amely egy bizonyos aggregált állapotban van. Normál körülmények között a gázban lévő molekulák közötti távolság tízszer nagyobb (lásd az 1.1. Bekezdést), mint méreteik; a legtöbb időt mozognak egyenes beavatkozás nélkül, a cselekvés, és csak jóval kisebb része az idő, amikor megtalálják követően a közeli távolságokban más molekulák, kölcsönhatásba lépnek velük, változó mozgás irányát. Így a gázszerű állapotban a molekula mozgása a 6a. Ábrán vázlatosan látható.
nagyon alacsony hőmérsékleten, a molekulák nagyon kicsi kinetikus energiával rendelkeznek, és a vonzási erők a molekulákat egy rendezett, szorosan lezárt struktúrában vagy rácsban tartják. Ebben az esetben a molekulák a kristályrács csomópontjai közelében (egyensúlyi pozíciókban) oszcillálnak, minél kisebb az amplitúdó, annál kisebb a hőmérséklet. Ha az energiát a kristályba viszik, hőmérséklete emelkedik, és a molekulák egyre inkább oszcillálnak az egyensúlyi helyzetükön. Ha a kristály hozta elegendő energiát, rendezett szerkezetét a molekuláris kristály megsemmisül-cal kinetikus energia a termikus mozgás a molekulák és a szabadon „siklik” mentén a másik, bár még mindig folyadékkal érintkező-sayutsya egymással. Ez a helyzet megfelel a folyékony állapotban, és a hőmérséklet közötti átmenet a kristályos és a folyékony-CoC-határozza nagyságrendileg egyenlettel határozzák meg kTpl = ep0. ahol Tm az anyag olvadáspontja. A folyadékot még mindig a vonzás ereje tartja meg, bár a molekuláknak elegendően nagy mozgási mozgási energiája van, hogy állandó egyensúlyi helyzetben maradjanak. Ha a folyadék, hogy korábban, emellett az energia molekulák elkezdenek mozogni elég gyors, és képesek legyőzni a gravitációs erő, teljesen elválasztva egymástól, és mozgó térben egy független úton. Ez a helyzet megfelel a gázállapotnak, és a folyadék és a gáz közötti átmeneti hőmérsékletet forráspontnak kell tekinteni.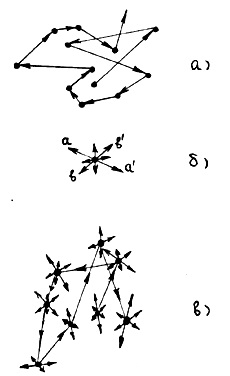
A szilárd állapotban, minden molekula (atom) az anyag egyensúlyi Xia helyzetben (rácspont), amely körül megy át a kis rezgések és az irányt (k-intézkedés AA „a 6. ábrán, b) és az amplitúdó hogy e rezgések véletlenszerűen változtatni (például a bb 'irányt) sokkal hosszabb idő után, mint ezeknek az oszcillációknak az időszaka; A különböző helyeken található molekulák rezgései általában nem azonosak. Egy egyedi szilárd állapotú molekula mozgásának pályáját általában a 6b. Ábrán vázoljuk.
A szilárd anyag molekulái olyan szorosan vannak csomagolva, hogy a köztük lévő távolság megközelítőleg egyenlő azok átmérőjével, azaz az r0 távolság a 2. ábrán. A tapasztalatból ismert, hogy a folyékony állapot sűrűsége körülbelül 10% -kal kisebb a szilárd anyag sűrűségénél, más dolgok egyenlőek. Ezért a folyadékállapotú molekulák közötti távolság némileg nagyobb, mint r0. Tekintettel arra, hogy a folyadék molekulái a Lada még nagyobb mozgási energia hőmozgást, várható, hogy ellentétben a szilárd állapotba, akkor, egy vibrációs mozgás, ez elég könnyű, hogy változtassa meg a helyüket, így a távolból, nem jelentősen meghaladó a molekula átmérője. A folyékony molekula mozgásának fő jellemzői a 6. ábrán vázlatosan mutatják. Így a mozgását molekulák egy folyékony egyesíti poszt-transzlációs mozgás, ahogy ez a helyzet a gáz, és rezgési megfigyelt szilárd állapotban.
Annak ellenére, hogy a molekulák mozgása egyenlőtlen a különböző aggregátumokban, ezeknek a mozgásoknak a véletlenszerűsége és kiszámíthatatlansága gyakori. Ezeknek a rendezetlen mozgásoknak az átlagos kinetikus energiája meghatározza az anyag hõállapotát és annak hõmérsékletét.