A kutatók egy csoportja új módszereket javasolt a gerincagyi atrófia kezelésére
A kutatócsoport a Laboratory, Cold Spring Harbor (CSHL) rávilágított a patológia spinális izomsorvadás (SMA) - egy ritka, de veszélyes betegség, amely izomgyengeséget és bénulást a fő genetikai halálok csecsemőknél. Új ötletek hasznosak lehetnek azon tudósok számára, akik jelenleg dolgoznak azon, hogy meghatározzák az optimális stratégiákat a betegek kezelésére a betegséggel.
Az SMA a motoros neuronok betegsége. Ez az idegek degenerációjához vezet, amelyek szabályozzák az izmokat és a tudatos mozgást. Ezeknek a neuronoknak szükségük van egy olyan fehérjére, amely a "motoros idegsejtek életképességének" (SMN) proteineként ismert. Általános szabály, hogy az összes sejt tartalmaz két fehérje változatot, az SMN1 és az SMN2. Egészséges betegeknél a sejtek gazdag SMN1-ben, és az SMN2 korlátozott számban van, és instabil alakja van.
Az SMA-ban szenvedő betegeknél a sejtek nem képesek SMN1 fehérjét termelni. Így kénytelenek az SMN2 fehérje kis mennyiségére támaszkodni.
Adrian Krainer professzor a CSHL-től, az Isis Pharmaceuticals-szel együttműködve olyan gyógyszert fejlesztett ki, amely lehetővé teszi az SMN2 gén megfelelő szerkesztését, ezáltal jelentősen megnövelve a funkcionális fehérje mennyiségét az idegsejtekben. Az antiszensz oligonukleotidot (ASO) ismert gyógyszert nagymértékben várták az SMA-val végzett laboratóriumi egerek klinikai vizsgálatokban. Jelenleg a CMA betegek klinikai vizsgálatai a 3. fázisban vannak.
A hatóanyag közvetlenül az SMA csecsemők és gyermekek cerebrospinalis folyadékához jut. "Úgy véltük, hogy az SMN létezésének területe a központi idegrendszerben (CNS) van jelen, és nem a perifériás szövetekben, mint a végtagok vagy a máj. Ezért a legtöbb erőfeszítésünk az SMN szintjének emelésére irányult a központi idegrendszerben "- magyarázza Krainer. "De az elmúlt években bizonyítást nyert, hogy kihívást jelent a betegség patológiájával kapcsolatos feltételezéseinkre, és van egy kérdésünk: növeljük-e a SMN szintjét a központi idegrendszerben vagy a perifériás szövetekben vagy két helyen egyszerre?"
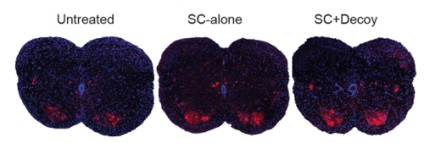
A génekben A fejlesztés arról számolt be, hogy a kutatók kifejlesztették a perifériás szövetekben a SMN-termelés helyreállításának módját, amely lehetővé teszi számukra, hogy meghatározzák a hatóanyag szerepét a központi idegrendszeren belül és kívül. A csapat laboratóriumi egereket kezelt a jól bevált ASO-val, szubkután injektálva. A korábbi eredmények szerint a hatóanyag növelte a SMN szintjét mind a központi idegrendszerben, mind a perifériás szövetekben. Újszülött egereknél a perifériára bevezetett hatóanyag eljuthat a központi idegrendszerbe. Ennek köszönhetően az állatokat meggyógyították.
Ezután a tudósok beadták a "csalit" oligonukleotidot a központi idegrendszerbe, és beadták az ASO-t az SMA zónába. "A csalikat a központi idegrendszerben kellett inaktiválniuk" - magyarázza Krainer. "Az SMN2-t még perifériás szövetekben állították elő, de nem nőtt a központi idegrendszer." De az eredmények meglepőek és előre nem látottak voltak. "Meglepődtünk, hogy felfedezhetjük, hogy a figuránknak nincs semmiféle hatása a motoros neuronokra és a gyógyulásukra. A kezdeti feltevéseinkkel ellentétben a központi idegrendszerben a SMN szintjének emelkedése nem nélkülözhetetlen laboratóriumi egerek, SMA betegek megmentése érdekében. "
Ez a munka segíthet az SMA kezelésének optimális stratégiáinak kidolgozásában. "Lehetséges, hogy a gyógyszer injekciójának megváltoztatása jobb eredményekhez vezethet. A laboratóriumi egerek egyedülálló jellegzetességeinek megfigyelései segítenek megérteni a fehérje alapvető mechanizmusát, és ez nagyon fontos "- mondta Krainer.
A következők alapján: www.cshl.edu
Illusztráció az oldalról: www.cshl.edu