Béta-laktám antibiotikumok - kémiai enciklopédia
b - LACTAMY ANTIBIOTICS. tartalmazzák a molekula b-laktám ciklusát. Gyakorlatilag minden természetes laktám antibiotikumot kivonunk a termelők tenyésztőfolyadékából. A mechanizmus az antibakteriális hatás, hogy blokkolja az utolsó lépés a szintézis baktériumok fala, ami a sejt lízist. Megkülönböztetni a biciklikus és a monociklikus laktám antibiotikumokat. Az elsőhöz csatlakoznak. egy k-ryh 4-tagú laktám gyűrűvel kondenzált az atomhoz N és egy szomszédos szénatomon egy 5-tagú heterociklus, - tiazolidin (habok), pirrolin (karbapenamy) és oxazolidin (oksapenamy) - vagy 6-tagú digidrotiazinovym gyűrűt (cefalosporinok és cefamycin). Penamák közé tartoznak a penicillinek - az első laktám antibiotikumok. széles körben beültetett mézbe. gyakorlatban. Ők gyártják gl. arr. Penicillium nemzetségből származó penészgombák. A penicillinek viszonylag könnyedén átjutnak a kémre. a p-laktám gyűrű megnyitásával jár. Naib. tanulmányozták benzilpenicillin vagy penicillin G (F-la I), és a fenoxi-metil. vagy V (II) penicillin. A benzilpenicillin majdnem elvesztette fontosságát, mint egy lek. Wed-in a rezisztens mikrobák terjedése miatt - a fertőzés kórokozói. A túlnyomó többsége ipari lemerült Stu benzilpenicillin előállítására használjuk a 6-amino to-meg (6-APA; f la III) jelenlétében enzimatikus hidrolízis. penicillin-aciláz, amelyet Escherichia coli termel.
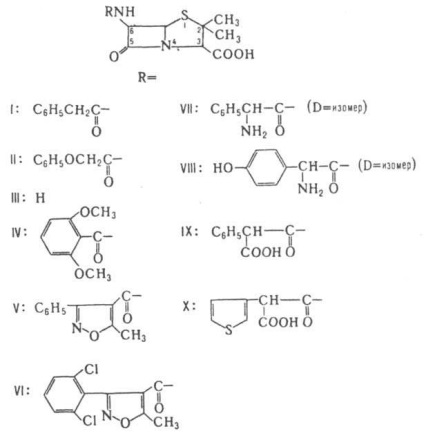
O. a penicillinek elnyomják a ch. arr. grampolozhit. baktériumok. Ezek az in-va érzékeny a inaktiváló b-laktamáz (penicillinázokat), és mások. Bakteriális enzimek hatására egy-b ryh nyitott laktám gyűrűt. Acilezése 6-APA, annak sói vagy észterei anhidridek vagy sav-kloridok, így a különböző T-polusintetich. penicillin. Synthesized St. 20 ezer származék, amelyből méz. Az alkalmazás csak keveset talált. tízes. Biol. sv-va semisynthetics. a penicillinek Ch. arr. a természet a szubsztituens a 6-helyzetben tehát az ellenállást a p-laktamázok biztosít terjedelmes szubsztituensek létrehozása sterich. a p-lakk ciklus szakadásának akadályai. Penicillinek NH2 - vagy COOH - csoport, az oldallánc általában egy széles hatásspektruma. Naib. széles körben használt meticillin (IV), oxacillin (V), dicloxacillin (VI), ampicillin (VII), amoxicillin (VIII), karbenicillin (IX) és ticarcillin (X). Egy nagy félszintetikus csoport. A penicillinek származtatott vegyületek. VII -. Azlocillin (XI), mezlocillin (XII), és a piperacillin (XIII), a csoporthoz tartozó ureidopenitsillinov és bacampicillin (XIV), hetacillin (XV), stb Ezek különböznek a szigetek emelkedett. Chem. stabilitás; Ezenkívül az ureidopenicillinek szélesebb spektrummal rendelkeznek, mint az ampicillin. Észterezett származékaik IX -COOH - acil szubsztituens csoport azonos spektrumú antibakteriális fellépés, mint az eredeti comp. de ellenállnak a b-laktamázoknak. A metoxilcsoport bevezetése a 6-os helyzetben erősen növeli a stabilitást, a temotsillinnel vagy a 6a-metoxi-karcillinnel (XVI). Amikor a tiazolidin-gyűrű S-atomját oxidáljuk a szulfonra, egy vegyület képződik. képes β-laktamáz gátlására.
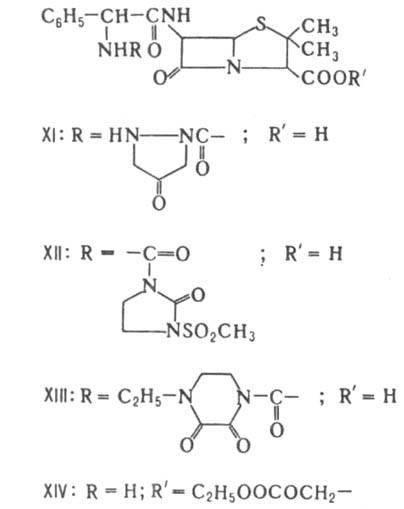
A penamam például amidipenicillint is tartalmaz. Mecillin (XVII), amely a penicillinektől különbözik egy összetettebb hidrolitikus mechanizmussal. felosztása. Conn. XVI és XVII elnyomja a preim. gramotritsat. baktériumok.
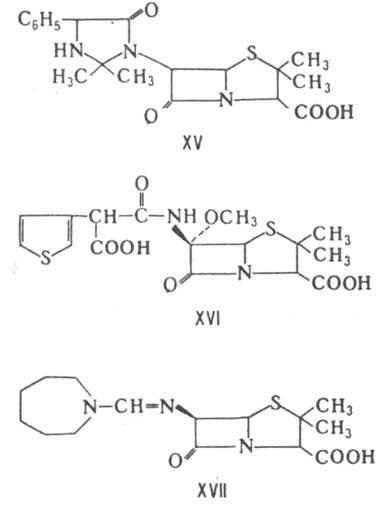
Carbapenam - vegyület. a XVIII. A termékek lebomlanak. a Streptomyces nemzetségbe tartozó mikroorganizmusok. Tartalmaz kb. 20 képviselő. Az antimikrobiális aktivitás széles spektruma és a b-laktamázok gátlására képes. A legtöbb karbapenám-származék hipotetikus. oliván k-ti [a XVIII általános képletben R = b-CH3CH (OH), R '= HOCH2CH2. n = 0]. Naib. Thienamicin [R = a-CH3CH (OH), R '= NH2CH2CH2 aktív. n = 0], carpetimycin A [R = b - (CH 3) 2C (OH), R '= CH 2 = CHNHCOCH 2. n = 1], PS-5 vegyület [R = a-CH3CH (OH), R '= CH3QO) CH2CH2. n = 0]. Az oxapenam naib. A Streptomyces clavuligerus által termelt klavulánsavat (XIX) tanulmányozták. Gyenge antimikrobiális aktivitással rendelkezik. számos b-laktamázzal szemben elnyomhat. Ezt a VIII. (Lecitin augmentin) -szel együtt alkalmazzák. Monociklusos. A laktám antibiotikumok közé tartoznak a. Nokarditsiny és mono-baktamy, valamint szintetikus. azetidinonok, elsősorban a monoszulfaktám. Chem. stabilitást és antimikrobás szereket
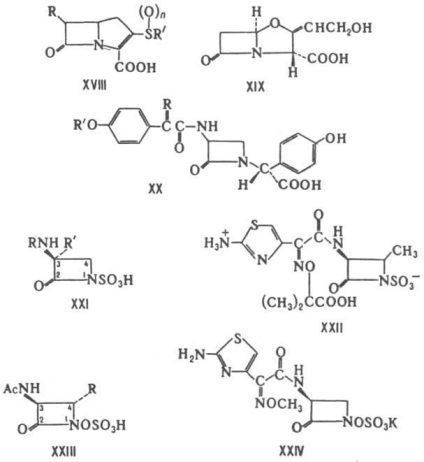
azzal jellemezve, aktivitása 2-azetidinonok terjedelmes az elektrondonor szubsztituensek az N atom a b-laktám gyűrűt. Az antimikrobiális hatás spektruma Ch. arr. helyzetű szubsztituense 3. Nokarditsiny (teljes p-la XX) által termelt nem-cardia uniformis subsp. tsuyamanensis. Szorítsuk meg a gramotritsat. baktériumok. Tartalmaz 6 képviselőt, naib. aktív amelyek közül az egyik nokarditsin A [be a XX általános képletű R = (Z) -NOH, R „= D-HOOCCH (NH2) CH 2 CH 2]. Monobaktámok (teljes p-la XXI; R „= H vagy OCH3) vannak a baktériumok által termelt a nemzetségek Acetobacterium, Gluconobacterium, Chromobacterium, Pseudomonas egyes fajok. Ezek az antibiotikumok viszonylag alacsonyak a gramotricatákkal szemben. baktériumok stabilak a b-laktamázokra. A szintetikus anyagokból. monobactam naib. érdeklődés származik L-treonin aztreonam (XXII), a-nek eltérő természetes magas antibakteriális aktivitással. Monoszulfaktamy - szintetikus. 2-azetidinonok (XXIII általános képlet, R = H vagy CH3). Viszonteladók. származékok L-szerin vagy L-treonin aminogidroksi-D-alanin és a SEQ. ciklizálás. O-szulfonálást és N-acilezést. Naib. A széles antibakteriális spektrumot a (XXIV) monoszulfát jellemzi. Irod A tudomány és a technológia eredményei, ser. Biológiai kémia. t. 19, ed. SM Navashina, M. 1983; Rosenfeld GS "Antibiotikumok és orvosi biotechnológiai", 1986, Vol. 31, №4, p. 302; A b-laktám antibiotikumok kémia és biológiája, ed. R. B. Morin, M. German, v. 1-2, N.Y. 1982 Cimarusti C.M. Sykes R. W. "Med. Res. Rev.", 1984, v. O., 4. o. 1-24. GS Rosenfeld.
