Mi a peptid
1900-ban a német szerves kémikus Hermann Emil Fisher előterjesztette azt a hipotézist, hogy a peptidek bizonyos kötések által létrehozott aminosav-láncból állnak. És már 1902-ben is megkérdőjelezhetetlen bizonyítékot szerzett a peptidkötés létezéséről, és 1905-ben kifejlesztett egy általános eljárást, amely lehetővé tette a peptidek laboratóriumi körülmények között történő szintetizálását.
Fokozatosan a tudósok tanulmányozták a különböző vegyületek szerkezetét, kifejlesztett módszereket polimer molekulák monomerekké történő elválasztására, egyre több peptidet állítottak elő. A mai napig több mint 1500 fajta peptid ismeretes, tulajdonságait meghatározták, és szintézis módszereket fejlesztettek ki.
A peptidek olyan molekulák, amelyek minden élő sejtben jelen vannak, és rendelkeznek a legkülönbözőbb biokémiai tulajdonságokkal. A peptidek két vagy több aminosavból állnak. A peptidmolekula az aminosavak szekvenciája: két vagy több aminosavmaradék, amidkötéssel összekapcsolva, peptidet képez. A peptid aminosavai száma nagymértékben változhat. És számuknak megfelelően különböztetik meg:
oligopeptidek - legfeljebb tíz aminosavmaradékot tartalmazó molekulák; néha nevük említi az aminosavak számát összetételükben, például dipeptid, tripeptid, pentapeptid stb.;
polipeptidek - molekulák, amelyek több mint tíz aminosavat tartalmaznak.
Több mint 100 aminosavmaradékot tartalmazó vegyületeket általában fehérjéknek neveznek. Azonban ez a részleg önkényes, néhány molekulát, például egy csak huszonkilenc aminosavat tartalmazó glükagon-hormont neveznek proteinhormonnak. A minőségi összetétel megkülönböztethető:
homomer peptidek - kizárólag aminosavmaradékokat tartalmazó vegyületek;
heteromer peptidek - olyan anyagok, amelyek nem fehérje összetevőket is tartalmaznak.
A peptidek az aminosavak összekapcsolásának módja szerint is fel vannak osztva:
homodetnye-peptidek, amelyek aminosav-maradékai csak peptidkötésekkel kapcsolódnak;
heterodéta peptidek - azok a vegyületek, amelyekben peptidkötések mellett diszulfid-, éter- és tioéterkötések is vannak.
Néhány peptidet szintetizálnak a sejt riboszómáiban a mátrix RNS transzlációja során, és ezután például hormonokká válnak. Mások enzimekké válnak. Ezenkívül vannak olyan peptidek, amelyek része a különböző receptorok szerkezetének, amelyek viszont hormonokkal és jelátviteli molekulákkal kapcsolódnak.
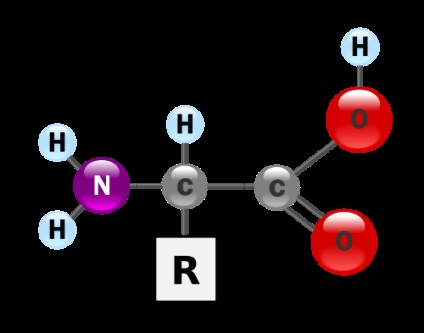
Az aminosavak kis molekulák, amelyek viszont atomokból állnak. Mindegyik aminosav több részre osztható, amelyek összetétele szükségszerűen két (aminocsoportot és karboxilcsoportot) tartalmaz. Az aminocsoport tartalmazza a nitrogénatomot (N), amely két hidrogénatomhoz kapcsolódik (H). Ez a csoport NH2-ként jelenik meg. A karboxilcsoport egy oxigén (O) és egy hidrogénatom (H) közül kettőhöz kötött szénatomot tartalmaz. Ez a csoport COOH-ként jelenik meg.
A fenti két atomcsoport között, az adott aminosavtól függően, az ilyen aminosavra egyedülálló atomok és vegyületek lesznek.
Különböző forrásokból tudjuk, hogy az emberi test, vagyis a sejtjei a peptidek bioszintézisében körülbelül 20 aminosavat használnak. Minden egyes genetikai kód jelzi, hogy az aminosavakból származó peptidek és fehérjék szintetizálódnak.
Glycine - Glycine - Gly - G
Alanin - Alanin - Ala - A
Valine - Valine - Val - V
Izoleucin - izoleucin - Ile - I
Leucin - Leucin - Leu - L
Proline - Proline - Pro - P
Szerin - szerin - Ser - S
Threonine - Threonine - Thr - T
Cisztein - Cisztein - Cys - C
Metionin - Metionin - Met - M
Aszparaginsav - aszparaginsav - Asp-D
Asparagin - Asparagin - Asn - N
Glutaminsav - glutaminsav - Glu - E
Glutamin - Glutamin - Gln - Q
Lizin - Lizin - Lys - K
Arginin - Arginin - Arg - R
Hisztidin - hisztidin - His - H
Fenilalanin - fenilalanin - Phe - F
Tirozin - tirozin - tir - y
Triptofán - triptofán - Trp - W
Attól függően, hogy a szervezet képes-e elődeinek aminosavakat szintetizálni, az aminosavak két csoportra oszthatók: Irreplaceable. Amelyek a következők: valin, izoleucin, leucin, treonin, metionin, lizin, fenil-alanin, triptofán, arginin, hisztidin. És cserélhető. Amelyek a következők: glicin, alanin, prolin, szerin, cisztein, az aszpartát, az aszparagin, glutamát, glutamin, tirozin.
Sokan tudják, hogy az alternatív helyettesíthető és helyettesíthető aminosavak besorolása nem hibák nélkül, de nem fogunk foglalkozni ezzel a problémával, de menjünk tovább.
Az aminosavak összekapcsolódnak egymással, úgynevezett peptidkötéssel. A peptid-kötés céljából egy amidkötés, amely alatt következik be a képződő fehérjék és peptidek eredő kölcsönhatását α-amino-csoport (-NH 2) egy aminosav a α-karboxil-csoport (-COOH) egy másik aminosavval.
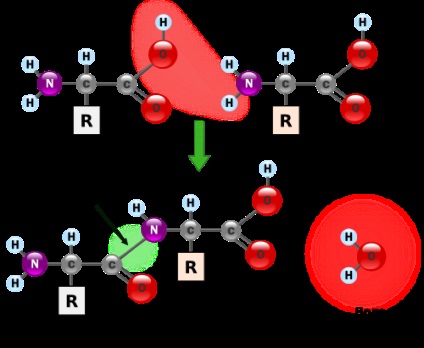
Az (1) és (2) két aminosavból egy dipeptidet (két aminosavból álló láncot) és egy vízmolekulát képezünk. Ugyanezzel a módszerrel a riboszóma hosszabb aminosav-láncokat is termel: polipeptideket és fehérjéket. A különböző aminosavakat, amelyek a fehérje "építőkövei", megkülönböztethetők az R radikális részektől.
Sok "kíváncsi elmék" gyakran találkoznak a világhálón a "peptidek" kifejezéssel. Tehát itt az endogén növekedési hormon szintézisére (és a sportra utalva) a következő peptidek tartoznak:
A növekedési hormon (GHRP) peptidek felszabadulása:
- GHRP-6 (His-DTrp-Ala-Trp-DPhe-Lys-NH2)
- GHRP-2 (DAla-D-2-Nal-Ala-Trp-DPhe-Lys-NH2)
- Hexarelin (His-D-2-metil-Trp-Ala-Trp-DPhe-Lys-NH2)
- Ipamorelin (Aib-His-D-2-Nal-DPhe-Lys-NH2) *
* Aib = Gamma-aminovajsav (GABA); D-2-Nal = "D" formájú 2-naftil-amin
A növekedési hormon hormonjainak felszabadulása (GHRH):
- A GHRH, vagy GRF (1-44) (Tyr-Ala-Asp-Ala-Ile-Phe-Thr-Asn-Ser-Tyr-Arg-Lys-Val-Leu-Gly-Gln-Leu-Ser-Ala-Arg-Lys -Leu-Leu-Gln-Asp-Ile-Met-Ser-Arg-GIn-GIn-Gly-Glu-Ser-Asn-Gln-Glu-Arg-Gly-Ala-Arg-Ala-Arg-Leu-NH 2) *
* a "féléletidő" ideje körülbelül 5 perc
- GRF (1-29) vagy Sermorelin (Tyr-Ala-Asp-Ala-Ile-Phe-Thr-Asn-Ser-Tyr-Arg-Lys-Val-Leu-Gly-Gln-Leu-Ser-Ala-Arg-Lys Leu-Gln-Asp-Ile-Met-Ser-Arg-NH2)
* a "féléletidő" ideje körülbelül 5 perc
D-Ala2 GRF (1-29) (Tyr-DAla-Asp-Ala-Ile-Phe-Thr-Asn-Ser-Tyr-Arg-Lys-Val-Leu-Gly-Gln-Leu-Ser-Ala-Arg- Lys-Leu-Leu-Gln-Asp-Ile-Met-Ser-Arg-NH2)
* A "felezési idő" körülbelül 10 perc, mivel a 2. aminosav alanin D-alaninnal
Módosított GRF (1-29) vagy a CJC-1295 lizin nélkül, és anélkül, DAC (Tyr-DAla-Asp-Ala-Ile-Phe-Thr-Gln-Ser-Tyr-Arg-Lys-Val-Leu-Ala-Gln-Leu -Ser-Ala-Arg-Lys-Leu-Leu-Gln-Asp-Ile-Leu-Ser-Arg-NH2)
* a felezési ideje kb. 30 perc a 2., 8., 15. és 27. aminosav helyettesítésével
CJC-1295 CJC-1295 vagy egy DAC (Tyr-DAla-Asp-Ala-Ile-Phe-Thr-Gln-Ser-Tyr-Arg-Lys-Val-Leu-Ala-Gln-Leu-Ser-Ala-Arg- Lys-Leu-Leu-Gln-Asp-Ile-Leu-Ser-Arg-Lys- (maleimidopropionil) -NH2)
* A "féléletidő" időszak több nap (hetek) az albuminmolekula hozzáadása következtében.