Fázisátalakulások és metastabil állapotok - a tökéletlen rendszer
Bizonyos körülmények között, két különböző fázisa egy anyag (például folyékony és gáz) létezhet együtt egymással tetszőlegesen hosszú ideig. Ehhez, a következő feltételek határán a két fázis:
Vezessük egyensúlyi feltételeinek egyes alapelveit disztribúciók!
Az első feltétel szükséges a termikus egyensúly, a második mechanikai egyensúly, és a harmadik az egyensúlyt a részecskék számát. Amikor akár bármilyen egyik ilyen körülmények között fázisok vagy a hőáram is létezni fog, akár a felület jár erő vagy részecskék mozog az egyik fázisból a másikba.
A kémiai potenciál kapcsolódik a Gibbs energia arány
A földgáz esetében a Van der Waals-erők is tartsa a vonalat, amely megfelel az egyensúlyi fázis. Ezt a vonalat nevezzük binodal. A helyzet a területek egyenlettel határozzák meg binodal levágta egy vízszintes vonal függően p (V).
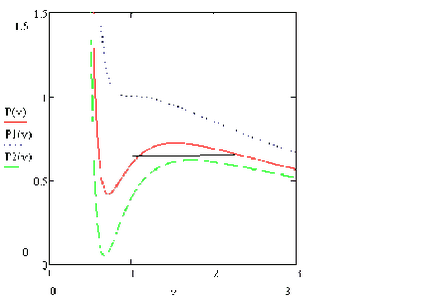
A megfelelő sorban szélsőérték pontokat különböző izotermák, az úgynevezett spinodal.
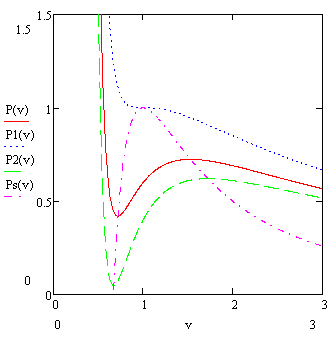
Meg lehet mutatni, hogy spinodal mindig belül binodal. Csakúgy, mint a spinodal, binodal mindig van egy maximuma a kritikus pont. Bent a spinodal egyfázisú állam nem lehet instabilitása miatt - mindig van egy kétfázisú állapot. Két spinodal egy régió metastabil állapotok. Azaz, államok, van egy véges idő alatt, ám a véletlen ingadozások idő múlását egy kétfázisú állapot. Egyfázisú együttélés görbe az a terület az államok, amikor a létezését kétfázisú állapotban lehetetlen.
Ha izoterm összenyomja a gázt Van der Waals erők, kezdve nagy mennyiségben, ez fog történni. Először a mennyiség lesz gáz (gőz), majd egy csepp a folyadék fog bekövetkezni, majd a folyadék lesz több és több, amíg nem veszi a teljes mennyisége. Akkor lesz csak a folyadék, amely gyakorlatilag összenyomhatatlan. Az átmenet a folyadék szilárd, vagy gáz halmazállapotú folyékony nevezzük elsőrendű átmenetet. Ebben az esetben az adott entrópia az anyag és a fajlagos térfogata nem folytonosak. Amikor a másodrendű fázisátalakulások, ezeket a mennyiségeket alávetni törés.
Azonban másik lehetséges forgatókönyv kapcsolódó létezését metastabil fázisok. Ebben az esetben, ha a rendszer nincs perturbáció, és az anyag szinte nincs szennyeződés egy izotermikus kompresszió a gáz való áttérés folyékony állapotban nem binodal és kevesebb mennyiség. Ez az állapot a pár az úgynevezett „túltelített”. Másfelől, a bővítése folyadék léteznek után binodal „túlhevített folyadék.” Mindkét államok metastabil, abban az értelemben, hogy azok stabilak a kis zavarokat, de instabil képest véges zavarokat. De mivel a zavar gyakran rendszertelenül, az utolsó merénylet előbb vagy utóbb. Ebben az esetben, a metastabil állapot bomlik, hogy létrehozzák a stabil fázis. Például, ha melegített víz forrásban lévő nem kezdődhet 100 0 C-on és ennél magasabb hőmérsékleten.
A főbb típusai a metastabil állapotok túlhevítés és a túlhűtés.
Túlhűtés - az anyagot lehűtjük alábbi egyensúlyi hőmérséklete átmenet egy másik fizikai állapot (fázis); egy speciális esete a rendszert egy metastabil állapotban. A szekvencia fázisátalakulások a magas vagy alacsony hőmérsékletű fázisokat (folyadékkristályos pár I kristály II) lehetőleg túlhűtés minden fázis tekintetében, hogy kövesse. Hypothermia szükséges, hogy a fázisátalakulás az 1. típusú történt véges sebességgel. Big túlhűtés homogén rendszerben lehet az oka, hogy a hiánya versengő fázisú sejtmagok vagy nagyon lassú növekedés miatt alacsony mobilitás molekulák.
amelyben az alábbi túlhűtés volt megfigyelhető fém cseppek - az egyensúlyi kristályosodási hőmérséklet: 52 K (Hg), 122 K (Sn), 296 ezer (Ge), 277K (Cu). A légkörben a víz is lehet a túlhűtött állapotban. Például, kis csepp víz lehet a légkörben folyékony állapotban legfeljebb -40 ° C-on
Túlmelegedés - fűtés a kondenzált fázisban hőmérsékletre egyensúlyi hőmérséklete fölé, a másik fázis, úgy, hogy a kezdeti fázis egy metastabil állapotban. Korlátozása túlmelegedés megfelel a spinodal. Folyadékok felszabadítással túlmelegedhet sokkal magasabb egyensúlyi hőmérséklet a gőz. A túlmelegedés lehet elérni nemcsak a növekedést. hanem a csökkenése külső nyomás, az alábbiakban.
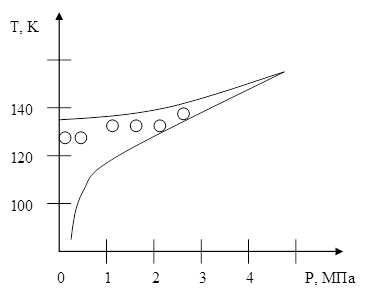
Az 5. ábrán körök jelzik kísérleti értékek forrásig argonatmoszférában homogén izobár melegítés egy üvegcsőben: az alsó görbe - telítési vonalon (binodal) felső görbe - spinodal.