állami funkciók
A funkciók az állam úgynevezett komplex fizikai mennyiségek kezelhetetlen közvetlenül mért és számított keresztül para-méter állapotban. A mérnöki termodinamika, az alábbi állami funkciók: belső energia, entalpia, entrópia.
Paraméterek és funkciók az állam a gázok mindig ugyanazt az értéket ebben az állapotban, függetlenül attól, hogy közben éri el a hűtés vagy fűtés, bővítése vagy kompressziós a gáz.
EnergieyU úgynevezett belső energia tartalék, amelyből obladaettelo egyensúlyban vannak. A folyamatok vizsgált műszaki termodinamika, változás belső energiával történő változtatásával az állomány belső termikus energia test, amely összege a kinetikus energia a transzlációs, rotációs és oszcilláló mozgás-gyulladásgátló szer molekulák és potenciális energiája azok inter-akció. Bent a kinetikus energia függ a testhőmérséklet és növekszik az azt. A belső potenciális energia függ a távolság a molekulák és növekszik, ha tömörítő-SRI, t. E. Ez attól függ, a nyomás és a sűrűség. Így a belső energia függvénye a paraméterek, amelyek meghatározzák a állapotban a test. Abban az esetben tökéletes gázok, amelyben nincs interakció kényszeríti molekulák változni fog a belső energia miatt egyetlen mérhető neniem-kinetikus mozgási energia a molekulák, azaz a. E. Az ideális gáz
Entalpia. Makroszkopikus test tulajdonságainak és viselkedésének kotoryhizuchaetsya termodinamika, összeköttetésben vannak a környező szerveket. A sor belső energia a test és a külső test energiája kölcsönhatás a környezet kombináljuk kifejezés „en-
A matematikai jelölés entalpia adják
ahol U - belső energia a rendszer; pv - a potenciális energia a közepes nyomást a rendszerben, kifejezve a rendszer beállításait.
Az ideális gáz állapotegyenlet (2.5) lehet a termék PV
helyébe RT. majd
A entalpiája ideális gáz attól függ, csak a hőmérséklete, t. E.
A belső energia és entalpia egységnyi tömegű vesche-TION, az úgynevezett specifikus (u és i), a mértékegység, amely J / kg.21
Az entrópia jelzi formájában energiát csere-teploty.Iz Menenius entrópia érték képviseli az előfordulása közötti hőcsere a rendszer és a környezet. Amikor a hőszolgáltató a szervezet növeli entrópia, visszahúzása során - csökken. Entrópia izolált rendszer egyensúlyban, akkor változatlan marad.
Entrópia jelöli S és egy dimenziója J / K; specifikus entrópia - a s. a dimenziója J / (kg · K).
Állami funkció u. i. s pozitív értéket. A termodinamika tanult technikai eljárások általában nem igényel meghatározására az abszolút értékeket, és elegendő ahhoz, hogy meghatározzuk csak ezek változásait mennyiségben. Ezért a referenciapontot u. i. s lehet a-nyat tetszőleges a rendszer állapotát. A termodinamika, hagyományosan feltételezzük, hogy az értékek a belső energia, entalpia és entrópia normál fizikai körülmények nulla.
Work változtatásával történik gáz állapotban számítjuk poformule
ahol p - gáznyomás, gáz jellemző erő hatása okra-természetes környezetre, Pa; V - gáztérfogat változás jellemző fur-nikai mozgó test határán m3.
A nyomás a termodinamikai rendszer az oka elkövetése pa-botok. Bővítése vagy kompressziós a gáz csak akkor lehetséges, ha a rendszer nyomása eltér a környezeti nyomás. Vegyünk egy jel-CIÓ munkát a változás a rendszer térfogata. A munka pozitív, ha a gáz kitágul, és negatív, ha a gáz összenyomódik.
Alkalmazott diagramot grafikai munka, Vai nevezett dolgozó, ahol a munka mennyisége által mért terület felett található a görbe a munkaközeg térfogata a folyamat (ábra. 2.1).
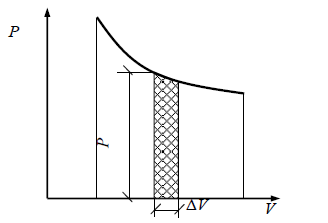
Ábra. 2.1. Grafikus ábrázolása a munka gáz (folyamatábra)
A hőt. A hőmennyiség, ami a rendszer kommunikál okra-természetes környezetre állapotának megváltoztatása határozzuk meg az expressziós
ahol T - a hőmérséklet; S - változás entrópia a rendszer.
A hőmérséklet is magában foglaló folyamat hőcserélő van Xia oka az energia csere a hő formájában. A hőcsere közötti-Lamy csak akkor lehetséges, ha a hőmérséklet-különbség.
A jel hőátadás a változás entrópia. Fokozott entrópia jelzi, hogy a rendszer a hőszolgáltató (hő-negatív-pozitív), csökken - a visszavonását hőt a rendszer (hő-negatív-negatív) entrópia összhang - melegítés nélkül.
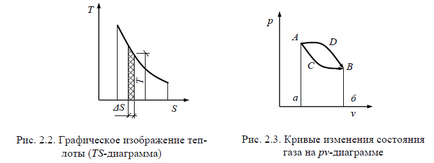
A grafikai hőmennyiség alkalmazott dia-gramm, úgynevezett hő, ahol a hőmennyiség mérhető Ploscha-a harmat a görbe alatti entrópia változást állapotváltozás a test (ábra. 2.2). Work és a hő, említett 1 kg gáz-vel jelöljük kisbetűket E, illetve L és Q és mértékegysége J / kg.
egy olyan rendszer állapot PV - TS -diagram és képviseli egy pont, és a folyamat - annak átmeneti ív a kezdeti, hogy a végső állapot.
Ábra. 2.3 A rendszer átmenet állapotban A és B állapotba-végrehajtására lehetnek különböző módon: a görbe ADV és DIA. Alatti terület ezen görbék különböző, ezért különböző, és a munka mennyiségét és sok TEP. Ugyanakkor a kezdeti és a végső állapotban a rendszer mindkét folyamat egyformán (A és B pontok).
Így a munka és a hő nyilvánulnak csak a folyamat Menenius államok és jellegétől függ a folyamat.
A termodinamikai rendszer fontos szerepet játszik vnut változás, belső energia, amely kifejezett a munka mennyiségét és a hő, amelyet cserélődnek ki a környezettel. Ebben a rendszerben növeli a belső energia, ha a hőt, (vagy több, a munka elvégzésének), és csökkenti a belső energia, ha hőt ad le, a környezetbe (vagy csinál munkát okra-természetes környezetre).
t. e. változás a belső energia a rendszer a különbség kitüntetéssel coli hő és a munka, amely a rendszer kommunikál a környezetet.
Más szóval, az összes dolgozó szállított folyadék a hő raskho-
duzzogás a változás belső energia és a munka elvégzésére, mert a hangerő változás: