Kén és jellemzői
Általános jellemzés kén
Kén - tizenhatodik elem a periódusos rendszer. Rendeltetése - S a latin «kén». Található a harmadik harmadban, VIA-csoport. Arra utal, hogy a nem-fémek. magtöltés 16.
Kén a természetben előfordul az szabad állapotban (natív kén), valamint a különböző vegyületek. Nagyon elterjedt kénvegyületek különböző fémekkel. Sok közülük értékes ércek (például, galenit PbS, cink cinkféle ZnS, kalkocit Cu2 S), és szolgálnak forrásként színesfémek.
Kénvegyületek a természetben is gyakori szulfátok, elsősorban a kalcium- és magnézium-Végül, kénvegyületek szereplő növényi és állati szervezetekben.
Atomi és molekuláris tömege a kén
Relatív molekulatömege az anyag (Mr) - egy szám mutatja, hogy hány alkalommal a tömeg a molekula már 1/12 tömeg szénatomot, és a relatív atomtömeg elem (Ar) - hányszor az átlagos súlya atomok kémiai elem nagyobb, mint az atomi tömege 1/12 szén.
Az értékek az atomi és molekuláris tömege a kén egybeesik; azok egyenlő 32,059.
Allotrópia allotropic módosítások és kén
Kén létezik két allotropic módosításokkal - rombusz és a monoklin.
Normál nyomáson kén formák rideg sárga kristályok, amelynek olvadáspontja 112,8 ° C; sűrűsége 2,07 g / cm 3. Úgy nem oldódik vízben, de jól oldható az szén-diszulfid, a benzol és más folyadékok. Elpárologtatására folyékony kén válik ki az oldatból, a sárga színű kristályok alakjában a rombos rendszer, amelynek az alakja octahedrons, amelynek általában része a sarkok vagy élek a darabolást (1. ábra). Ez a módosítás az úgynevezett rombusz kén.
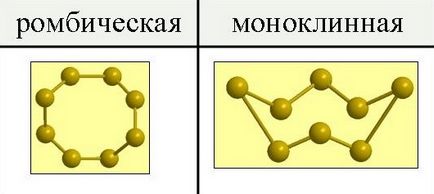
Ábra. 1. allotropic módosítása kén.
Egyéb formái kristályokat kapunk lassan lehűtve olvadt kén, és amikor azt részben megszilárdul egyesítése még nem volt ideje, hogy megszilárduljon a folyadék. Ilyen körülmények között, az edény falak bélelt belső, hosszú sötét sárga tű kristályok monoklin rendszer. Ez a módosítás az úgynevezett monoklin kén. Sűrűsége 1,96 g / cm 3. olvadáspontja 119,3 ° C, és az csak stabil feletti hőmérsékleten 96 ° C-on
kén izotópok
Ismeretes, hogy a természet a kén lehet formájában négy stabil izotópok 32 S, 33 S, 34 S, és 36 S. Tömegük számok 32, 33, 34 és 36, ill. A atommag kén izotóp S 32 tartalmaz 1616 protonok és a neutronok, és a 33 S izotópot, 34 S, és 36 S- protonok száma megegyezik, tizenhét, tizennyolc, húsz neutronok rendre.
Van mesterséges kén izotópok tömegszáma 26-és 49-perces, a legstabilabb jelentése S 35 egy felezési egyenlő 87 nap.
A külső energia szintjét a kénatom hat elektronok, amelyek a vegyérték:
1s 2s 2 2 2 2p 6 3s 3p 4.
Ennek eredményeként a kémiai kölcsönhatás közötti kén elveszíthetik vegyérték elektronok, azaz legyen a donor, és át pozitív töltésű ionok vagy felvesznek elektronokat egy másik atom, vagyis legyen az elfogadó, és légy negatív töltésű ionok:
S 0 → S 6+ -6e;
S 0 → S -4e 4+;
S 0 → S -4e 2+;
S o + 2e → S 2-.
Molekulát és egy kénatom
Egyatomos kén-molekula - S. bemutatunk néhány jellemző tulajdonságok kénatom és molekula: