Vizsgálat szerkezete és tulajdonságai fázisok fémötvözetek
Az Oktatási Minisztérium és a Tudományos Ukrajna
Donbass Állami Műszaki Egyetem
fegyelem „Kohó”
„Szerkezete és tulajdonságai fázisok fém ötvözetek. A szilárd oldatok kémiai vegyületek. A heterogén szerkezet”
1.Fazy fémötvözetekben
Az ötvözet olyan anyag, olvasztásával kapott két vagy több elem (fém vagy nemfém fémekkel).
Komponensek - kémiai elemek alkotó ötvözet.
Úgynevezett homogén fázist (homogén) rendszerkomponensek, azonos összetételű, kristály szerkezete és tulajdonságai egy és ugyanazon aggregált állapotban, és el van választva a többi része a felület.
Szerkezete alatt megértésében az alakja, mérete és jellege a kölcsönös elrendezése a fázisok a fém vagy ötvözet.
Ötvözetlen szerkezeti összetevők, azaz különálló részből az ötvözet, amelynek ugyanaz szerkezet sajátosságait figyelembe. Az ötvözetek szerinti fizikai-kémiai kölcsönhatás a komponensek alkotják a következő fázisokat: folyékony oldatok, szilárd oldatok, a vegyi anyagok és közbenső fázisok. Tekintsük az ötvözetek szilárd állapotban.
2.Mehanicheskie keverék
Mechanikai keveréket - a két komponens, A és B van kialakítva, akkor, ha nem tudják, hogy kölcsönös a szilárd anyag feloldódik, és nem reagál kémiailag vegyületeket nyerjük. Az ötvözet áll kristály komponens, A és B (ábra. 1).
1. Ábra mechanikai keverékéből mikroszerkezet
A mechanikai tulajdonságok függnek az aránya a komponensek. Példák ötvözetek, amelyben a mechanikai keverék képződik: Fe-Pb, Pb-Si.
3.Tverdye megoldások
A szilárd oldatok úgynevezett fázisok, amelyben a komponensek egyike az ötvözet megtartja kristályrácsban, és más atomok (vagy egyéb) komponensek el vannak rendezve a rács az első komponens (az oldószer), a változó méretek (időszakok). Így, a szilárd oldatot, amely két vagy több komponens, egy rácsos típusú, és egyfázisú.
A szilárd oldat létezik a tartományban komponens-koncentrációk.
Megkülönböztetése helyettesítő és szilárd oldatok oldatok (ábra. 2).
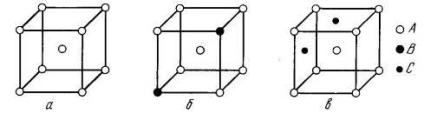
2. ábra reakcióvázlat szilárd oldatok: A - tiszta fém; b - szubsztitúciós szilárd oldatot; a - szilárd oldat
Ezeket a megoldásokat jellemzi vas-szén ötvözött acél, öntöttvas.
A formáció a szubsztitúciós szilárd oldat oldott atomok helyettesíti az oldószer egy részét atomot tartalmaz a kristályrácsban. Helyettesíteni lehet minden olyan atom.
A formáció a szilárd oldatot az oldott atomok található a hézagokban (üregek) a kristályrács az oldószer (ebben az esetben szükség van egy bizonyos üres teret). A nagy pórusok 0,74-0,41 R, kis pórusok 0,68-0,291R.
Az FCC - rács atomok vannak elrendezve egy oktaéderes pórus (rácsok központok). Ebben a pórusok elfér gömb sugara 0,41R, ahol R - sugara atom a rács.
A BCC - rács atomok rendezett egy tetraéderes hézagokban, pórusok mérete (0291 R).
Atomjai az oldószer és az oldott anyag eltérő méretű, így a formáció a szilárd oldat kristályrács mindig torz, és az ő időszakok változhat.
A formáció a helyettesítő szilárd oldat osztásperiódus növelheti vagy csökkentheti. A formáció a szilárd oldat az oldószer rács időszakban mindig növeli (ábra. 3).
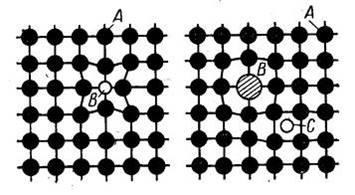
3. ábra A torzítás a kristályrács képződése során helyettesítő szilárd oldat és bevezetése
Az atomok oldott anyag gyakran felhalmozódó diszlokációk, csökkentve azok elasztikus energiát (ábra. 4).
Interstitialis atomok olyan területen helyezkedik el feszített alatt a szélén a extra, amely egy úgynevezett Cottrell atmoszférában (ábra. 4).
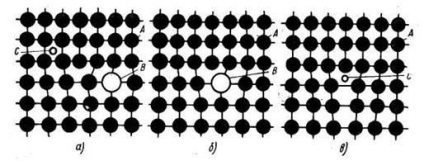
4. ábra képződése Cottrell légkör: A - atomok B komponenst alkotó szubsztitúciós szilárd oldatot, és S. alkotó atomok szilárd oldatot, véletlenszerűen elrendezett egy rácsos komponens; b és c-atomok a B és C komponens áttér a diszlokáció, miáltal a rácsenergiája alsó
Minden fémek különböző mértékű lehet oldjuk egymással, az ilyen szilárd állapotban: Al legfeljebb 5,5% Cu; A Cu és 39% Zn.
A szilárd oldatok zamesheniya korlátlan (bármilyen arányban) oldhatóság (. 5. ábra) lehet kialakítva felsorolt körülmények között az alábbiakban:
1. A komponenseket kell azonos típusú (izomorf) kristályos rácsok. Csak ebben az esetben koncentrációjának változtatásával a szilárd oldat lehet folyamatos átmenet a kristályrács az egyik összetevő a másik komponenshez rács.
2. A különbség atomi méretű (# 916; R) komponenseket kell a kis, és nem haladja meg a 8-15%.
3. A komponenseket kell tartoznak az azonos csoportba tartozó elemek a periódusos rendszer, vagy a szomszédos kapcsolódó csoportok, és a szerkezet közelében a elektronhéjak atomok.
5. ábra: A kristályrács A szubsztitúciós szilárd oldatok korlátlan a komponensek oldhatósági
Példák ötvözetek, amelyben van kialakítva egy folyamatos sorozata szilárd oldatok:
Cu (29) és a Ni (28) (# 916; R = 2,7%),
Fe és Co - nem oldódnak.
Bemutatjuk szilárd oldatok képződnek csak azokban az esetekben, ahol az átmérő az oldott anyag elem alacsony atomok (RVN. Al. / Rrastvor> 0,59).
Szilárd ilyen típusú oldatok úgy állítjuk elő, csak a fém (Fe, Mo, Cri stb) szén (atomrádiusz 0,77A °), a nitrogén (0,71A °), hidrogén (0,46A °), azaz . elemek egy kis atomrádiusz.
Szilárd interstitialis megoldások csak akkor lehet korlátozni a koncentráció, mivel a pórusok száma a rács korlátozott, és az atomok a fő komponens tárolja a rács csomópontok.
Rendezett szilárd oldatok
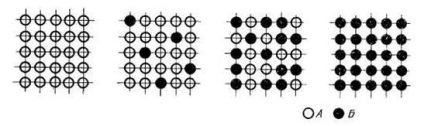
A ötvözetek Cu és Au, Fe és Al, Fe és Si, Ni és Mn, alkotó magas hőmérsékleten helyettesítési megoldások elemeinek elhelyezésére neuporyadochnnym atomok, a lassú hűtés vagy melegítés, megvilágítási folyamat újraelosztása atomok tart, magasabb hőmérsékleten. Ennek eredményeként, melynek összetevői atomok foglalnak el bizonyos pozíciókat (ábra. 6) a kristályrácsban. így képez rendezett szilárd oldat vagy a felépítmény.
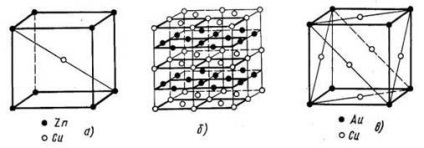
6. ábra kristályrácsba rendezett szilárd oldatok: egy - CuZn, b - CuAu, in - Cu3 Au
Oktatási felépítmény módosítások kíséretében tulajdonságai (például az ötvözet Permalloyból (vas- és 78,5% nikkel) rontja a mágneses permeabilitás, megnövekedett keménység és csökkentett duktilitását ellenállás változások).
Rendezett oldatok képződnek, amikor az arány a komponensek az ötvözet (at.%) Állandó: 1: 1 (CuAu); 1: 2; 1: 3 (Cu3 Au); stb (Kémiai képlet lehet tulajdonítható, hogy a vegyület CuAu, Cu3 Au).
Rendezett szilárd oldatokat úgy kell tekinteni, mint az intermedier fázis közötti a szilárd oldatok vagy kémiai vegyületek.
A rendezett szilárd oldatok az oldószer rács megmarad, de van egy megfelelő az atomok elrendezése és faragott változtatni jellemző tulajdonságait a kémiai vegyületek.
4. Kémiai vegyület
Vegyszerek és a kapcsolódó természet fázisok fémötvözetekben sokfélék. Jellemzői kémiai vegyületek:
1. A kristályrács rácsok eltér az alkatrészek az ízületet alkotó. Atomok vannak elrendezve rendezett módon. Kémiai vegyületek folyamatos kristályrács (ábra. 7).
2. A vegyület mindig tárolva egyszerű többszöröse a komponensek aránya, amely lehetővé teszi számukra, hogy kifejezzék a képlet: A n Bm, A és B-komponensek; n és m- prímszám.
3. A kapcsolat tulajdonságait ritkán térnek el a tulajdonságait alkotóelemét. Cu - NV35; Al - NV20; CuAl2 - NV400.
4. Az olvadási hőmérséklet (disszociációs) állandó.
5. A kémiai vegyület képződése kíséri jelentős termikus hatása.
Kémiai vegyületek képződnek a komponensek között, amelynek nagy a különbség az elektron szerkezete az atomok és kristályrétegeiben.
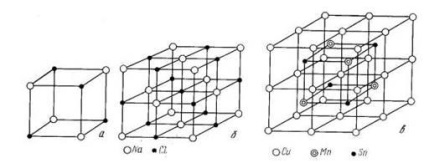
7. ábra: A kristályrács: a, b - vegyületet NaCl, into- vegyületet Cu2 MnSn (Box 8 áll réz atomok, 4 mangán atomok és az ón atomok 4)
Egy példa a tipikus kémiai vegyületek normál vegyértékkel szolgálhat Mg-vegyület elemekkel IV-VI gruppPeriodicheskoysistemy: Mg2 Sn, Mg2 Pb, Mg2 P2. Mg2 Sb2. Mg3 Bі2. MgS és mások. Egyes vegyületek más fémekkel ismert intermetallikus vegyületeket. Kémiai kötés intermetallikus vegyületek általában fém.
Számos kémiai vegyületek alakult fémötvözetek, eltérő néhány jellemzőjét a tipikus kémiai vegyületek, mert nem engedelmeskedik a törvényei vegyérték és nincs állandó személyzet. Tekintsük a legfontosabb kémiai vegyületek alakult ötvözetek.
Átmeneti fémek (. Fe, Mn, Cr, Mo, Ti, V, W, stb) képeznek egy nem-fémek C, N, H vegyületek: karbidok (C), nitridek (s N), boridok (B), hidridek ( H). Gyakran nevezik intersticiális fázisok.
bevezetése fázis képletű:
MX (WC, TiC, VC, NBC, TiN, VN és mtsai.).
A kristály szerkezete intersticiális fázisok által meghatározott nem-fém atomrádiuszok (Rx) és fém (Rm).
Ha az Rx / Rm <0,59, то атомы металла в этих фазах расположены по типу одной из простых кристаллических решеток: кубической (К8, К12) и гексагональной (Г12), в которую внедряются атомы неметалла, занимая в ней определенные поры.
bevezetésével fázis erősen: elektromos vezetőképesség, olvadáspont és nagy keménység.
bevezetésével fázis alkalmazásával, amelynek kristályrácsban eltérő a rács az oldószer fém.
Alapján intersticiális fázisok könnyen képez szilárd oldatok kivonó (VC, TiC, ZrC, NBC), néhány atom a rács csomópontok hiányzik.
Ezek a vegyületek képeznek közötti monovalens (Cu, Ag, Au, Li, Na) fém vagy átmeneti fém (Mn, Fe, Co és mtsai.), Egyrészt, és egyszerű fémek egy vegyértéke 2-5 (Be, Mg , Zn, Cd, Al, stb), a másik oldalon.
Az ilyen típusú vegyületek (azonosított angol Metal Hume - Rothery), azzal jellemezve, hogy egy bizonyos arányban a vegyérték elektronok az atomok számát: 3/2; 21/13; 7/4; Minden arányt felel meg határozott kristályrácsban.
Tekintettel 3/2 BCC rács van kialakítva (jelzi # 946; - fázis) (kocka, CuZn, Cu3 Al, 5 CU Sn, szén, Feal).
Amikor 21/13 összetett köbös rács (52 atom sejtenként) - # 947; - egy fázis (5 CU Zn8 Cu31 SN8 Cu9 AL4 Cu31 Si 8-ig ...).
Ha 7/4 elérhető közel hexagonális rács, jelöljük # 949; - fázis (CuZn3 CuCd3 Cu3 Si, Cu 3 Sn, Au3 Sn, 5 CU Al3 ..).
Elektronikus kapcsolat megtalálható számos technikai ötvözetek - Cu, Zn, CuiSn (ón) FeiAl, Cu és hasonlók Sii Jellemzően, a rendszer figyelhető mind a három fázis (# 946;, # 947;, # 949;).
Bizonyos vegyületek elektronikus atomarány, a kristályrácsban különböző komponensek rácsok - kémiai jellemzői. vegyületek. Azonban, a vegyületek egy rendezett az atomok elrendezése. A hőmérséklet csökken (a melegítés után) egy részleges rendelés, de nem teljes. Az elektronikus komponensek vegyületet kapjunk, amely a szilárd oldatot a széles koncentráció tartományban.
Így, ez a fajta vegyületek kell tekinteni a közvetítők között, a kémiai vegyületek és szilárd oldatok.
Táblázat №1 - elektronikus kapcsolat
Elektronikus csatlakozások különböző rendszerek: Cu - ZnCu - SnCu - ALCU - Si
Ezek a képlet AB2. vannak kialakítva arányban atomi átmérők komponensek IGEN / ET = 1,2 (általában 1,1-1,6). Laves fázisok hcp hexagonális rács (MgZn2 és MgNi2, BaMg2. MoBe2. TiMn2), vagy egy FCC (MgCu2. AgBe2. CaAl2. TiBe2. TiCr2). Ezek a fázisok egyaránt előfordulhat erősítő intermetallikus fázisok szuperötvözetek.
5. heterogén szerkezetűek
Ötvözetek heterogén (heterogén) szerkezet van kialakítva, ahol a komponensek nem rendelkeznek teljes körű kölcsönös oldhatósága. Növelésével a maximális oldhatóságot kapunk egy szerkezet, amely telített oldatok vagy szilárd oldat vagy kémiai vegyület.
Példák a rendszerek (Pb-Sb, Cu-Bi, Zn-Sn, Pb-Sn, Pb-Bi, Ni-Cr, Fe-C, Al-Cu, stb). Mindegyik fázisban kristályrácsába.
1. Lahtin YM VP Leontyev Anyagtudomány. M. 1972 1980
2. Gulyaev AP Fémtani. M. 1986
3. Sidorin II Alapjai anyagok. M. 1976
4. antikainen PA Fémtani. M. 1972
Hála az alkotók a honlapon! Vegyünk egy kis szünetet, diák szórakozni: A diákok átmennek a vizsgán a fizikában. Vesztes nagyon rosszul. A professzor megpróbálja húzza, megkérdezi: - Nos, mondj legalább az a hőmérséklet, amelynél a víz forrni kezd? - Professzor, nem tudom, hogy milyen hőmérsékleten felforrt, de tudom, hogy a 40 fokos válik vodka! By the way, az anekdota veszünk chatanekdotov.ru