Réz és vegyületei
A tanulság 11. természettudományos CLASS
Hogy fokozza a kognitív tevékenység és függetlenségét diákok, használjuk a tanulságokat a kollektív tananyag. Ezeken a leckék, minden tanuló (vagy pár diák) van rendelve, a végrehajtás jelentést kell ugyanabban az osztályban, és a jelentés rögzíti a többi diák osztály notebook és egy elem tartalma az anyag a leckét. Minden tanuló hozzájárul a tanulmány az osztály téma.
Az órán a diákok változó műveletet intraaktivnogo (üzemmód, amelyben az információáramlást belül zárt gyakornokok tipikus önálló munka), hogy az interaktív (üzemmód, amelyben az információáramlást, a kétoldalú, azaz az információ is a diák, a diák, információcsere). A tanár ebben az esetben működik, mint a szervező a folyamat, kijavítja és kiegészíti a jelentett adatok a diákok.
Lessons kollektív tananyag áll a következő szakaszokból áll:
Stage 1 - A telepítés, amelyben a tanár elmagyarázza a célját és működését program egy leckét (7 perc);
2. szakasz - önálló munka a diákok az utasítás (15 perc);
Harmadik szakasz - az információcsere és eredményeit összefoglalva a lecke (tart minden fennmaradó időben).
Lecke „Réz és vegyületei” célja osztályokban való intenzív vizsgálat Chemistry (4 óra Kémia hét), tartott két akadémiai óra, az óra frissített ismereteket hallgatók a következő témákban: „Általános tulajdonságok a fémek”, „kapcsolat fémek tömény kénsavat , salétromsav, „” Qualitative reakció aldehidek és többértékű alkoholok „” oxidációs korlátozó egyértékű alkoholok réz-oxid (II) »,« komplex vegyületek. "
Mielőtt a leckét, a hallgatók házi feladat: megismételni a felsorolt témákban. Előzetes felkészülés a tanár a leckét az, hogy ki oktatási kártyákat a diákok és oktatócsomagok laboratóriumi kísérletek.
A tanár határozza meg a hallgatók a célja a leckét. A meglévő ismeretek az anyagok tulajdonságait, megjósolni, ellenőrizze a gyakorlatban összefoglalják információkért a réz és vegyületei.
A hallgatók alkotják képletű email réz atom megállapítására, hogy milyen fokú oxidáció lehet rézvegyületek, amelyek tulajdonságai (oxidációs-redukciós, sav-bázis) lesz egy rézvegyület jelenlétében.
A táblázat jelenik meg a notebook a diákok.
A tulajdonságai réz és rézvegyületek
Ahhoz, hogy megerősítik és kiegészítik a feltételezések diákok végre laboratóriumi kísérletek az utasításokat, és írja egyenletek a reakció.
Útmutató az önálló munkavégzésre párban
1. kalcinált rézdrót a lángban. Figyeljük meg, hogyan változott színe. A forró kalcinált rézhuzal kerül etil-alkoholban. Megjegyzés: a változás a színét. Ismételjük meg ezt 2-3 alkalommal manipuláció. Ellenőrizze, hogy a szag etanol megváltozott.
Record két reakció egyenletek megfelelő transzformációk elvégzett. Milyen tulajdonságokkal réz és réz-oxid által támogatott ezek a reakciók?
2. A réz-oxid (I) mn sósavval.
Mit érdemes megnézni? Jegyezzük fel a reakció egyenletek, figyelembe véve, hogy a réz-klorid (I) - oldhatatlan vegyület. Milyen tulajdonságokkal réz (I) megerősítette ezeket a reakciókat?
3. a) réz-szulfát-oldatot (II) helyezze a cink granulátum. Ha a reakció nem megy végbe, az oldat hőmérsékletét. b) Ahhoz, hogy a réz-oxid (II) mn 1 ml kénsavat és a hő.
Mit érdemes megnézni? Írja le reakció egyenletek. Mik a tulajdonságait rézvegyületet megerősíti ezek a reakciók?
4. A réz-szulfát-oldatot (II) helyezzük a szalag Univerzális indikátor.
Magyarázza az eredmény. Record ionos egyenlet hidrolízissel szakaszban.
Előállítása nátrium-karbonát dagály méz-szulfát-oldatot (II).
Mit érdemes megnézni? Record egyenlet együttes hidrolízisét reakció a molekuláris és ionos anyagok.
5. réz-szulfát (II) mn fölös nátrium-hidroxid.
Mit érdemes megnézni?
Ahhoz, hogy ez a csapadék dagály ammónia-oldattal.
Milyen változások történtek? Írja le reakció egyenletek. Milyen tulajdonságokkal rézvegyületek bizonyul végzett reakciókat?
6. réz-szulfát (II) oldatot kálium-jodid dagály.
Mit érdemes megnézni? Készíts egy reakcióegyenlet. Mi az a tulajdonsága, réz (II) azt bizonyítja, ez a reakció?
7. A kémcsőben 1 ml tömény salétromsavat Place egy kis darab rézhuzal. Zárja le a fiola dugóval.
Mit érdemes megnézni? (Vegyük a cső alatt volt tapadás.) Rögzíti a reakcióegyenlet.
Egy másik csőbe öntjük sósavval, tegyük egy kis darab rézhuzal.
Mit érdemes megnézni? Magyarázd meg észrevételeit. Milyen tulajdonságokkal réz által támogatott ezek a reakciók?
8. Réz-szulfát (II) mn fölös nátrium-hidroxid.
Mit érdemes megnézni? A kapott csapadékot hőt. Mi történt? Írja le reakció egyenletek. Mik a tulajdonságait rézvegyületet megerősíti ezek a reakciók?
9. réz-szulfát (II) mn fölös nátrium-hidroxid.
Mit érdemes megnézni?
Ahhoz, hogy ez a csapadék dagály glicerin-oldat.
Milyen változások történtek? Írja le reakció egyenletek. Mik a tulajdonságai rézvegyületek mutatnak ezek a reakciók?
10. réz-szulfát (II) mn fölös nátrium-hidroxid.
Mit érdemes megnézni?
Ahhoz, hogy ez a csapadék dagály glükóz-oldat és a hő.
Mi történt? Jegyezzük fel a reakcióegyenlet, a általános képletű aldehidek, hogy jelezze a glükóz
.
Milyen tulajdonsága a rézvegyület bizonyítja ezt a reakciót?
11. réz-szulfát (II) dagály: a) egy oldatot ammónia; b) a nátrium-foszfát-oldat.
Mit érdemes megnézni? Írja le reakció egyenletek. Milyen tulajdonságokkal rézvegyületek bizonyul végzett reakciókat?
A tanár feltesz egy kérdést a tulajdonságait egy adott anyag. Diákok, akik hasonló kísérleteket végzett, erről beszámol kísérletet, és rögzíti a reakciókat a táblán. Ezután a tanár és a diákok teljes az információkat a kémiai tulajdonságait az anyag, ami lehetetlen volt, hogy erősítse meg a válaszokat egy iskolai laboratóriumban.
A sorrend, amelyben a kémiai tulajdonságait rézvegyületek
1. Mivel a réz reagál savakkal, réz képes reagálni, amit más anyagokkal?
Felvett egyenlet réz reakciók:
• a koncentrált és hígított salétromsav:
• tömény kénsav:
• sósav oxigén jelenlétében:
2. Milyen tulajdonságokkal rendelkezik-oxid és réz-klorid (I)?
Felhívjuk a figyelmet, hogy ± bázis tulajdonságai, a képesség, hogy komplexeket képeznek, redox kettősség. Felvett egyenlet réz-oxid reakciók (I):
• sósavat képezve CuCI:
CuCl + HCI = H [CuCl2];
• redukciós reakciók és oxidációs Cu2 O:
• diszproporcionálódást fűtési:
3.Which tulajdonságokat mutat-oxid a réz (II)?
Felhívjuk a figyelmet, hogy ± bázis és oxidáló tulajdonságai vannak. Felvett egyenlet réz-oxid reakciók (II):
CuO + 2H + = Cu 2+ + H2 O;
4. Milyen tulajdonságok réz-hidroxid, réz (II)?
Felhívjuk a figyelmet, hogy az oxidatív, ± bázis tulajdonságai, a képesség, hogy komplexeket képeznek mind szerves, mind szervetlen vegyületek. Felvett a reakciók:
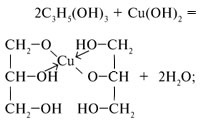
• egyenlete a bomlási reakció:
5. Milyen tulajdonságok mutatnak egy rézsó (II)?
Felhívjuk a figyelmet, hogy az ioncserélő reakciót, hidrolízis, oxidatív tulajdonságok, komplexképzéssel. Felvett egyenlet réz-szulfát reakciók:
Cu 2+ + Zn = Cu + Zn 2+;
és a reakciókat:
Cu 2+ + HOH = CuOH + + H +;
• közös hidrolízis nátrium-karbonáttal kialakítjuk a malachit:
Ezen kívül lehet mondani, a hallgató a kölcsönhatás a-oxid és -hidroxid réz (II) lúggal, ami bizonyítja amfoter jellege:
Összefoglalva: oxidatív tulajdonságai rézvegyületek növekednek a növekvő oxidációs fok. A rézionok komplexet tudnak képezni. A vegyületek a réz mutatjuk ± bázis tulajdonságai, bár a oxid és hidroxid réz (II) sztringens körülmények között reagálhatnak lúgokkal, bemutatva gyenge amfoter.
A fennmaradó óraszámban lehet költeni gyakorlatok és megoldására számítási problémák.
1. gyakorlat végrehajtása a lánc transzformációk:
2. Gyakorlat Javasolj legalább nyolc módon megszerezni a réz-kloridot (II).
2CuCl = CuCI 2 + Cu,
3. gyakorlat: Készíts egy lánc átalakítások, amelyek megfelelnek az alábbi programok és azok végrehajtására:
Probléma 1. A ötvözet réz alumínium oldatához előbb feleslegben alkálifém, majd fölös mennyiségű híg salétromsavat. Számítsuk ki a tömegarányai fém ötvözet, ha ismert, hogy a gáz mennyisége kivált mindkét reakcióban (azonos körülmények között), egyenlő
[1, p. 237, № 1464].
Probléma 2. kalcinálás, 6,05 g kristályos réz-nitrát (II) kapunk 2 g maradékot kapunk. Határozza meg a kiindulási só képletű [2, p. 204, № 836].
Probléma 3. A rézlemez lesüllyed súlyú 13,2 g 300 g vas-nitrát-oldatot (III) sót tömegű frakció 0,112. Amikor kivettük, azt találtuk, hogy a tömeghányada vas-nitráttal (III) egyenlő súlyú frakció a kapott réz-só (II). Határozza meg a súlya a lemez után azt kivesszük az oldatból a [2, p. 204, № 841].
Házi feladat. Ahhoz, hogy megtanulják a felvett anyagot a notebook. Létre láncreakció a vegyületek réztartalmú legalább tíz reakciók, és végrehajtja azt.