Lejáratú papírok kézhezvétele salétromsav
Salétromsav - az egyik legfontosabb ásványi savak. A termelés a vegyiparban ez a második csak a kénsav. A salétromsav előállítására széles körben használják számos termék használt ipar és a mezőgazdaság:
· Körülbelül 40% -a annak a fogyasztás a komplex és a nitrogén műtrágyák;
· A salétromsav előállítására használják
· Szintetikus gyógyszerek szerek stb.;
· Iron könnyen oldódik híg salétromsavban. Koncentráció salétromsav képződik a készítmény felületén a vas vékony, de sűrű réteg oldhatatlan tömény savas oxid, amely megvédi a fémet a további korróziótól. Ez a képesség, hogy passivate vasat használunk, amely megvédi a korróziótól.
Korábban, amikor nem volt a szintetikus ammónia, salétromsav kész volt fellépés kénsav a chilei-nitrát. Termelés térfogatok nagyon kicsik, és a savat használunk csak a robbanóanyagok előállításához, színezékek és egyéb vegyi termékek. Most salétromsavat előállított szintetikus ammónia és feldolgozott főként nitrogén műtrágyák.
Jellemzése alapanyag
Az alapanyag előállítására salétromsav az ammónia, a levegő és a víz.
Szintetikus ammóniával kisebb vagy nagyobb mértékben szennyező anyagokat. Ezek a szennyeződések a katalizátor por, a kenőolaj (kompressziós dugattyús kompresszor). A tiszta gáz alakú ammóniát elpárologtatjuk, és desztillációval állomás elválasztó folyékony ammóniát. További tisztítást végezzük egy szűrő, amely egy lencse alakú elemek, amelyben a szűrő anyag pamut velúr. Finom tisztítás ammónia-levegő keverék a szűrőben van kitéve porolitovymi csövekbe.
A légköri levegőt használják a termelés a salétromsav, úgy ez a gyári vagy közelébe. Ezt a levegőt szennyezett gáz halmazállapotú szennyeződéseket és a port. Ezért alaposan tisztítani, hogy elkerüljék mérgezés az ammónia oxidációs katalizátor. A tiszta levegő végezzük általában a gázmosó, öntözött vízzel, majd két-lépcsős szűrő.
Víz használható folyamat igényeinek, vetjük alá, hogy egy speciális készítmény: iszap mechanikai szennyeződésektől, szűrés és kémiai tisztítás oldott sók. A reakcióképes salétromsavat tisztításához szükséges gőz kondenzátum, amely tovább tisztítottuk lehetséges szennyeződések. [AM Kutepov, str.397]
Vízmentes salétromsav HNO3 nehéz színtelen folyadék pl.1,52 (15 ° C-on), füstölgő levegőben. Ez megfagy -41 és forr 86 ° C-on Forráspont sav kíséri részleges bomlás:
4HNO3 - 2H2 + 4NO2 + O2 - 259,7 kJ
A menekülő nitrogén-dioxid feloldódik a savban, a színei a sárga vagy vörös (attól függően, hogy az összeget a NO2) színes. Mivel salétromsavat vízzel keverik bármilyen arányban. hőleadás során salétromsav vízzel való hígítás, jelezve a hidrátok képződésének (HNO3 × H2O, HNO3 × 2H2O).
Salétromsav - erős oxidálószer. Fémek, azzal az eltéréssel, Pt, Rh, Ir, Au, tömény salétromsav, átalakíthatók a megfelelő oxidok. Ha az utóbbi oldódnak salétromsavban, nitrátok vannak kialakítva. [Muhlenov, p.99]
Kémiai fogalom módszer
A gyártási folyamat híg salétromsav három szakaszból áll:
átalakítása ammóniával nitrogén-oxid
4NH3 + 5O2 = 4NO + 6H2O (4.1)
oxidációja nitrogén-monoxid a-dioxid
a víz felszívódását a nitrogén-oxidok
4NO2 + O2 + 2H2O = 4HNO3 (4.3)
Az oxidációs hogy ammóniát oxigénnel a levegő csak akkor lehetséges, anélkül, hogy a katalizátor a N2.
A katalizátort a következő reakciók mennek végbe ammónia és oxigén:
4NH3 + 5O2 = 4NO + 6H2O; # 61508, H = - 946kDzh (4.1)
4NH3 + 3O2 = 2n2 + 6H2O # 61508, H = - 1328kDzh (4.4)
Ammónia oxidációs reakciókat kíséri jelentősen csökkenthető a szabad energia áramlik nagy sebességgel, gyakorlatilag visszafordíthatatlan. Hő a reakció során képződő, ez elegendő ahhoz, hogy a folyamat autoterm.
A katalitikus oxidációját ammóniával - többlépéses heterogén katalitikus folyamatban előforduló külső diffúziós régió és a korlátozott diffúziós ammónia katalizátor felületén.
Az alkalmazott katalizátorok a oxidációját ammóniával kell szelektív tulajdonságokkal, azaz felgyorsítja csak egy reakció. A legaktívabb és szelektívebb katalizátor platina. Ez is egy kis gyújtási hőmérsékletű
200 ° C, jó alakíthatóság, alakíthatóság. De a hátránya - ez a gyors megsemmisítése magas hőmérsékleten hatása alatt nagy nagy sebességű áramlás a reagensek és a katalizátor mérgek. Ez vezet a veszteségek a drága katalizátor és felszabadulását nitrogén-oxid, amely volt az oka a platina-ötvözetek más fémekkel. A legszélesebb körben következő katalizátorok (GOSZT 3193-59): Pt + 4% Pd + 3,5% Rh - üzemben atmoszferikus nyomás és Pt + 7,5% Rh - magasabb nyomáson. Katalizátorokkal formájában rácsok. Ez a forma kényelmes használni, és a kapcsolódó minimális fém költségeket.
A katalizátorok igen érzékenyek számos szennyezések az ammónia és a levegő, különösen fluorid vegyületek, és a kén. A szennyeződések jelentősen csökkenti a katalizátor szelektivitását. Ahhoz, hogy stabil a konverziós aránya szükséges alapos tisztítás ABC [1], és a mechanikai szennyeződések, különösen a vas-oxidok és a por a vas ammónia szintézis katalizátor. Az élettartama legfeljebb 14 hónapon át atmoszferikus nyomáson és emelt 9.
A hőmérséklet van a legnagyobb hatással a hozam a nitrogén-oxid (II). Ahogy a hőmérséklet növekszik NO kimenet növekszik, és létezik egy optimális hőmérsékleten (tiszta platina 900-920 ° C), amelynél a maximális hozamot. Nagy jelentősége van a gyulladási hőmérséklete a katalizátor, amely nagymértékben függ az összetétel. A platina, a reakció indul 195 ° C-on A kitermelés eléri a 96% a tiszta platina és 99% a ötvözetek. Eljárás végrehajtása során magas hőmérsékleten a növelése mellett a hozam a nitrogén-monoxid más előnyei: sebességének növelése az ammónia oxidációs reakciót, és csökkenti az érintkezési időt. De a hőmérséklet emelkedésével növekszik a veszteség drága platina azaz romló az eljárás gazdaságosságát.
A növekvő nyomás megfigyelt csökkenésnek a hozam a nitrogén-oxid (II). Azonban, a nagy nyomású javítja a teljesítményt a készülék, hogy csökkentse berendezés méretét. Az eljárást végezzük nyomáson 0,41-0,73 MPa. Ennek legfőbb feltétele megszerzésének magas NO kimenetek nyomás hőmérséklet-emelkedés és az érintkezési idő (számának növelése hálók).
Amikor a sztöchiometrikus arány az oxigénnel és ammóniával O2: NH3 = 1,25, légköri nyomáson, a nitrogén-monoxid-termelés 60 - 80%. Ezen kívül, azt lehetett volna dolgozni a területen robbanásveszélyes koncentrációt. Arányának növelésével az O2: N 1,7, amely megfelel a tartalmát az ammónia elegyében 11,5%, kitermelés: NO vozrastaet.d.lya megkapjuk a magas hozamok NO igényel 30% feleslegben oxigént a fenti sztöchiometriai. Ez annak a ténynek köszönhető, hogy a felület a platina katalizátor folyamatosan kell borított oxigénnel, vagy akár 500 ° C-on bomlani kezd ammónia nitrogén és az oxigén.
A oxidációja nitrogén-oxid (II)
2 NO + O2 2NO2; # 61508, H = - 124 kJ (4,2)
reverzibilis hogyan halad térfogatának csökkenését, és kíséri hőfejlődés. Ezért, a hőmérséklet csökkenése miatt, és a nyomás növelésével elősegíti a kialakulását a NO2. A hőmérséklet akár 100 ° C-on az egyensúlyi reakció szinte teljesen elfordultak jobbra.
2NO (NO) 2; # 61508, # 61512, # 61472, # 61500, # 61472, # 61488, (4.5)
# 61.519; 2 + (NO) 2 2NO2; # 61508; # 61512; # 61500; # 61.488, (4.6)
Így, a csökkenés a nitrogén-oxid oxidációs sebesség-dioxid a hőmérséklet növekedésével magyarázható erős koncentrációjának csökkenését a dimer. Jellemzően, a feldolgozás nitrózus gázok hőmérsékleten a 10 - 50 ° C-on, amely a polimerizált része dioxid N2 # 61.519; 4. Így, nitrózus gázok belépő abszorpciós tartalmaznak NO2, N2O4, NO, N2O, N2, N2O3.
Felszívódás nitrogén-dioxid
Minden nitrogén-oxidok, azzal az eltéréssel, NO, vízzel reagálva képeznek salétromsavat. Salétromossav vegyület instabil és bomlik salétromsav, nitrogén-oxid (II) és a víz. Felszívódás szerint zajlik a rendszer:
2NO2 + H2O HNO3 + HNO2; # 61508; # 61512; # 61472; # 61501; # 61472; # 61485; # 61489; # 61489; # 61494; kJ (4.7)
3HNO2 HNO3 + 2NO + H2O; # 61508; # 61512; # 61472; # 61501; # 61472; # 61495; # 61494; kJ (4,8)
Összesen NO2 vízzel reagálva a reakció a következő egyenlet szemlélteti:
3NO2 + H2O 2HNO3 + NO; # 61508; # 61512; # 61472; # 61501; # 61472; # 61485; # 61489; # 61491; # 61494; kJ (4.9)
A határréteg a gáz-folyadék átmenet bekövetkezik NO2 a folyékony fázisban. Ezután, a kémiai reakció (3) után történik NO2 oldódás, amely, szemben a diffúziós folyamat viszonylag gyorsan. Továbbá, a folyékony fázis viszonylag lassú bomlás salétromossav szerinti reakció (4). A kapott NO részlegesen oxidáljuk az oldatból az oxigént, de a legtöbb esetben - a gázfázisban. Lassú folyamat, meghatározzuk a felszívódás mértéke a nitrogén-oxidok azok diffúzió a gázfázisban.
Az abszorpció mértéke dioxid vizes oldataival salétromsavat nitrogén olyan tényezők határozzák meg, mint például hőmérséklet, nyomás, savkoncentráció. Amikor a hőmérsékletet csökkentjük, és a sav koncentrációja, és a nyomás növeli a konverziós ráta a nitrogén-dioxid növekszik. Amikor a salétromsav koncentrációja 65% feletti felszívódás majdnem megáll. Továbbá, a mértéke az NO konverzió NO2 függ a szabad térfogat, és az abszorbeált nitrogén-oxidok - a felületről a folyadékkal érintkező gáz. Ezért az egyik alapvető követelményeket a felszívódás berendezés, - létrehozása maximális üregtérfogatot egyidejűleg igen fejlett elnyelő felületek.
A nyersanyag olcsó és könnyen hozzáférhető szintetikus ammónia, amely ha optimálisan választott paraméterei lényegében minden megy a nitrogén-monoxid; A reakció irreverzibilis és gyors, és nem igényel anyagvisszavezetést. Alkalmazása megnövekedett nyomás csökkenti a berendezés mérete és a termelékenység növelését, de a hőmérséklet emelésével és mennyiségű katalizátor rácsok. Annak biztosítása érdekében, a kibocsátás a nitrogén-oxid több, mint 98% nyomáson 0,41-0,71 MPa, a hőmérséklet meghaladja a 950 ° C-on, de az érintkezési idő kisebb nem lesz 1,1 × 10-4 s, és a gáz sebessége több mint 160 liter / perc. Általában a hőmérséklet emelkedése növeli a hozamot, de ez vezet a nagy közvetlen veszteségek drága katalizátor.
Kiválasztásának indoklása folyamat paramétereinek
ABC betápláljuk a kontaktor nem tartalmazhat több, mint 10%, különben a katalizátort nem fedezi teljes mértékben az oxigén, és az oxidációt az ammónia, hogy kezd a nitrogén. Bár a lehető legmagasabb koncentrációja az ammónia, amely megvalósítja a magas hozam 11,0-11,5%, ha kisebb, mivel a gáz sebessége nagy, és a szükséges árrés áttörést. Az átalakítás a hőmérsékleten 870-900 ° C és a nyomás a 0,716 MPa. Ezeket a paramétereket választottuk alapján gazdasági mutatók, pl. Hogy. Növekedése a hőmérséklet növeli mind a hozam, és a közvetlen veszteség platina katalizátor.
A reakció NO oxidációs NO2 kezdenek végezzen hőmérsékleten 170 ° C, elegendő ahhoz, hogy jó kitermeléssel és a sebesség. Mivel a reakcióhő felmelegszik 300 ° C-on Az oxidáció mértéke körülbelül 85%. A felszívódását nitrogén-dioxid végezzük hőmérsékleten 35-40 ° C, mert ez eltolja az egyensúlyt, a jobb, a sav koncentrációja a kimenetnél eléri 55-58%.
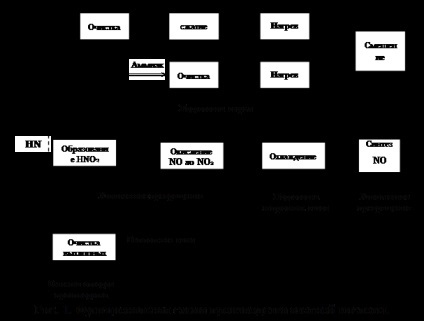
Funkcionális rendszer a salétromsav.
Az 1960-as, a gép gyártására tervezték salétromsav 120 ezer. T / év alatti nyomás 0,716 MPa segítségével nagy katalitikus tisztítására kipufogógázok, termelő termékek formájában 53-58% -os HNO3. Folyamatábra gyártási egyszerűsített kiviteli alaknál a 2. ábrán látható.
A légköri levegőt alaposan megtisztítjuk a kétfokozatú szűrő 1. A tisztított sűrített levegő kétfokozatú kompresszor. Az első szakaszban 18, a levegő összenyomódik a 0,35 MPa, miközben melegítjük 165-175 ° C miatt adiabatikus kompresszió. Lehűlés után levegő irányul, hogy a második kompressziós szakasz 16, ahol a nyomás növekedésével a 0,716 MPa.
A fő levegőáram tömörítés után a levegő melegítjük előmelegítőben 12 hő 250-270 ° C-on nitrogéngáz és betáplálják a keverő ammóniával keverőben 6.
Conversion ammónia zajlik platina-ródium rácsra hőmérsékleten 870 # 8209; 900 ° C, a konverziós foka 96%. Nitrózus gázok át 890-910 ° C-on adja meg a hőhasznosító kazán 15 alatt elhelyezett érintkező egységet. A kazán miatt a hűtés nitrózus gázok 170 ° C-on párolog kémiailag tisztított oxigénmentesített vízzel ellátó hőhasznosító kazán; így a gőz egy 1,5 MPa nyomáson és a hőmérsékletet 230 ° C-on, amely ki a fogyasztó számára.
Miután a visszanyerő kazánba nitrózus gázok belépnek az oxidálógáz nitrózus gázok 13. tartalmaz egy üreges egységet, melynek a teteje a van szerelve egy üvegszálas szűrőn csapdázására platina katalizátor. Részben nitrózus gázok oxidációs történik, hogy már a visszanyerő kazánba (40%). Az oxidálószer 13, az oxidáció mértékét növeljük 85%. Mivel az oxidációs reakciókat nitrózus gázokat melegítjük 300-335 ° C-on Ezt a hőt használják a levegő-előmelegítő 12.

A hőcserélőben lehűtjük 12 nitrózus gázok át további hűtés 11 hőcserélővel, ahol van egy csökkenés a hőmérséklet 150 ° C és a fűtés a kipufogógáz (farok) gázok a 110-125 ° C-on Ezután nitrózus gázok irányul hűtőszekrényben, a 7 kondenzátor, cirkuláltatott vízzel hűtött. Így kondenzvíz képződött gőz és a gyenge salétromsavat. Nitrogén elválasztott gázt a kondenzált salétromsav a 8 leválasztó, amelyből a salétromsavat tápláljuk be az adszorpciós torony 9 6-7-én lemez, és a nitrózus gázok - az alsó lemez az abszorpciós oszlop. Fent Az oszlopot lehűtjük gőz kondenzátum. Alakult tetején oszlop alacsony salétromsav koncentrációja áramlik az alsó lemezhez. Az elnyelés következtében a nitrogén-oxidok koncentrációját a sav fokozatosan növeljük, és eléri a kimenetet
1%. Ennélfogva a sav arra irányul, hogy a leürítő oszlop 10, ahol az előmelegített levegőt nyer átöblítjük nitrogén-oxidok, salétromsav és fehérített belép a raktárban. A levegő, miután az öblítés oszlop aljába tápláltuk az abszorpciós oszlop 9.
Így, ez az egység teljesen önálló energia. Energiát nyerünk vissza a felállítása ugyanazon tengelyen, mint a gázturbina turbófeltöltő. [Kutepov str.410-411].


Kiszámítása anyagmérleg XTC
4. Muhlenov IP És mások. Általános vegyészmérnök: A tankönyv. kémiai-technikai. spec. egyetemeken. A 2 m. T.2. A legfontosabb a vegyipari termelés / M. ügyvezető. wk. 1984 - 263 A.
[1] ABC - ammónia-levegő keverék.
[2] NG - nitrózus gázok.