Hoffmann reakciók - kémiai enciklopédia - szótárak és enciklopédiák
Hofmann reakció. 1) Az átalakítás, az amidok karbonsav-primer aminokká lehasadása CO2. bekövetkezik az intézkedés alapján alkálifém hipohalitok (Hoffmann-átrendeződés, Hofmann hasítása amidok):
Ahhoz, hogy egy vizes alkálifém p-Py hipohalit hozzáadott amid: Seq. melegítés 40-80 ° C-on teljessé a p-CIÓ. Ahhoz, hogy a hozam növelése aminok amidokká magasabb zsírsav p-t-CIÓ végezzük alkoholos p-D. Uretánok így kialakított könnyen hidrolizál-aminok. Az első szakasz GR-N-szintézis galogenamida képző hatása alatt az instabil alkálifémsójával I:
. Lépés meghatározó G. ráta p, - halogénatom hasítási alkotnak nitrén II, a-ing stabilizált átrendeződéssel egy izocianát:
Utoljára a kölcsönhatás. H2O keresztül-karbaminsav, hogy a konvertált. egy amin:
Azt találtuk, hogy a vándorló csoport elmenti a konfigurációt. Diffúz értelmében az amid anionját III kölcsönhatást. csatlakozó. tartalmazó elektrofil. többszörös kötések, például.
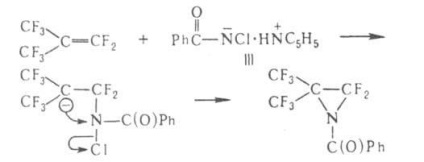
Amidygidroksikislot inenasyschennyh a-t alatt G. p. konvertált. aldehidek, amidok szubsztituált propionsav k a m-nitrilek amidyatsilaminokislot - in atsilglioksalidony:
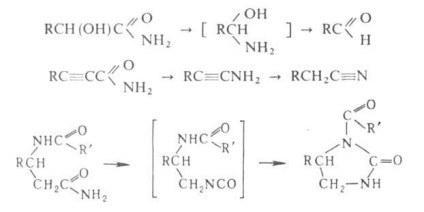
H. o. lehet jó kitermeléssel alifatich. zsírsav aromás. aromás. és geterotsiklich. aminok, diaminok és aminosavak; a prom-sti G. o. szintéziséhez használt antranilsavalkil hogy Te.
P-ció nyitott A. V. Gofmanom 1881.
2) bomlása kvaterner ammónium bázisokat, melyeknek a szénlánc egyik atomja N-atom vpolozhenii N, hogy egy tercier amin, olefin, és vizet (Hoffman felosztása):
Általában végzett bepárlásával, vizes vagy alkoholos p-ra tetraalkilammónium-hidroxid (gyakran vákuumban) egy fokozatos növekedése r-ry, hogy 100-150 ° C-on Használata keverékét vízmentes DMSO és THF csökkenti a T-py r-CIÓ szobahőmérsékletre. Ha az N-atom társított december alkil szubsztituensek, a DOS. olefin képződik a legkisebb számú alkilcsoportok a kettős kötés (jellemzően Hoffman), például.
Szubsztituensek priuglerodnom atom párosodni képes, és növeli kislotnostvodoroda (pl. Fenil) hasításának megkönnyítését az olefin. Ha több kötés vpolozhenii otscheplyaetsyaatom hidrogénatom és 1,4-eliminációs következik be, pl.
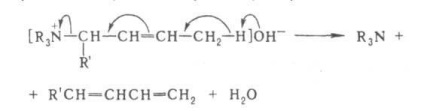
Abban az esetben, hogy két konjugált kötések vpolozhenii 1,6-elimináció és formázott trién pl.
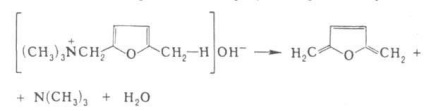
G. o. általában zajlik mechanizmusán keresztül bimolekulás megszüntetésére és sztereospecifitását bizonyos esetekben egy intramolekuláris gyűrűs. mechanizmust például.
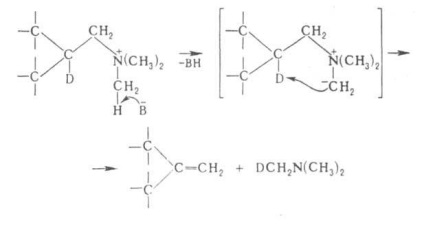
ahol B - a alapjai.
Major oldalán folyamatok kialakulása során GR-alkoholok, valamint éterek, epoxidok, származékai THF és ciklopropán. A p-CIÓ, mint G. o. írja szulfoniumsók és foszfóniumsók, pl.
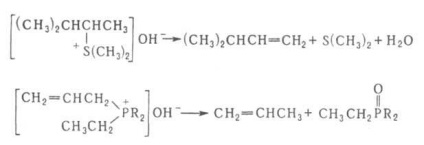
G. o. szintéziséhez használt telítetlen vegyületek. A szekvenciális metilezése aminok és ezek bontási (t. Úgynevezett. Kimerítő metiláció) azonosítására használt aminok.
P-ció nyitott A. V. Gofmanom 1851.
Lit.: Kop AK Tumbull ER Szo Organic Reactions, Acad. az angol. Szo 11, M. 1965. pp. 327-500; Mal Pass DR a könyvben. Általános Organic Chemistry, Acad. az angol. Vol. 3, M. 1982. o. 68-71. NP Hamparian.