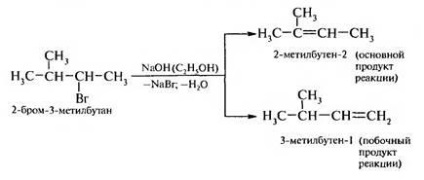
eliminációs reakció 2
Sok különböző módszerek bevezetésének egy halogénvegyület egy molekulába. Tekintsük a leggyakoribb.
1. halogénezése alkánok. A kölcsönhatás a alkánok halogénatommal keresztül megy végbe a szabad gyökös mechanizmussal SR során UV-besugárzás.
A hátránya ennek a módszernek, a kialakulása egy mono-, di- és poligalogenalkanov.
2. A csatlakozás a hidrogén-halogenidek, hogy alkének. A reakció szokásos, de a hideg, hogy az eljárás különösen alkalmas monogalogeno- származékok, mivel a reakciót nem kíséri semmilyen mellékhatás-by-poligalogenoproizvodnyh termékek.
elektrofil addíciója - AE reakció mechanizmusára.
3. A reakciót az alkoholok halogénezőszerekkel. Gyakran halogénszármazékok történő helyettesítésével kapott a hidroxilcsoportot halogénatommal alkoholok. Erre a célra, halogenidek (HC1, HBr, HI), foszfor-halogenidek (RS13. RS15. RVg3. RVg5), tionil-klorid (SOCI2).
A kölcsönhatás alkoholok hidrogén-halogenidekkel továbblép séma szerint:
A legegyszerűbb módja halogénatommal szubsztituált hidroxilcsoportot terc-Nogo szénatomos. Végezzük el a reakciót a primer alkohol nem szükségszerűen, a katalizátorok jelenlétében: ásványi savak, a cink-halogenidek, stb ...
A magasabb hozamok halogénalkánok kialakítva köl-kölcsönható alkoholok foszfor-halogenidek (111) vagy foszfor (V), és a tionil-klorid:
4. A reakciót a halogén-alkánokat hidrogén-halogenidekkel sók Kitty csomó (Finkelshteina reakció). A reakció előállítására használt fluoratom vagy több, hozzáférhető yodalkanov klór- vagy bróm:
Az alsó halogén-alkánok - gáz vagy folyadék egy jellegzetes édes illata, közepes - folyékony, magasabb - szilárd vesche-CIÓ. Legtöbbjük vízben gyakorlatilag oldhatatlan, de könnyen oldódik szerves oldószerekben.
Halogén-alkánok rendelkeznek nagy reaktivitása, és jellemzi őket nukleofil szubsztitúció (SN), pel-kitermelés (hasítás) (E). Azt is reagálnak a Sun-képződés és kölcsönhatásba léphet bizonyos fémek.
Nukleofil szubsztitúciós reakciók
Halogén-alkánok képessége, hogy vegyenek részt okozott reakciókat SN polaritású szén-halogén kötések. halogénatom, amelynek elektronegativitási nagyobb szénatom, keverjük össze az elektron-sűrűség kommunikációs ronnuyu C-Hal. Ennek eredményeként, halogénatom priobre olvadáspontú részlegesen negatív töltéssel (# 948, -), a szénatom, - részleges pozitív töltést (# 948; +). Halogén-alkánok reagálnak nukleofil reagensekkel, így szubsztitúció van az n-logena nukleofil.
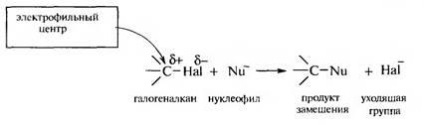
Attól függően, hogy a szerkezet a halogénalkánt, a természet a nukleofil és a reakció-oldószer S fordul elő két fő irányban Yam: SN 1 és 2 Sn.
SN 2 mechanizmus (bimolekuláris nukleofil szubsztitúció)
A mechanizmus a SN 2 primer és reagálnak valamivel nehezebb WTO hexadecimális halogén-alkánok. A reakciót egy lépésben keresztül Obra-mations az átmeneti állapot. Kezdetben, a nukleofil támadás atom yr-leroda kapcsolódó halogén- (elektrofil centrum), a másik oldalán a C-Hal. t. e. a támadás hátulról. Az eredmény fokozatos elmozdulás egy nukleofillel halogenidion (kilépő csoport). Ez a folyamat egy átmeneti állapot, azaz a. E. idő, amikor a kötvény C-Hal még mindig nem szakadt, és a C-Nu kötés még nem alakult ki teljesen.
Kialakulása az átmeneti állapot kíséri változás-em hibrid állapottal szénatomon sp 3 sp nA 2. Egy frakciót negib- ridizovannoy p atomi egy szénatom az átmenet az álló rész-orbitális átfedés a támadó nukleofil la, és a második - halogénatom orbitális .
Visszatérve szénatomok sp3 -Hybrid-állami hasítás után halogenidion jönnek konfiguráció inverziója megy végbe.
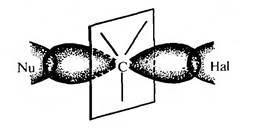
Reakciói a SN 2 mechanizmus az aktív nukleofil reagensek - ezek könnyebben képeznek átmenetet-készlethez, amely - és aprotikus oldószerek, protikus poláros oldószereket, mint szolvatált nukleofil, ezáltal csökkentve a képességét rea Zion.
A javaslatot a brit kémikus K. Ingold leírt mechanizmus megkapta a kijelölési SN 2. Az S betű azt jelzi, helyettesítéssel, N - a típusú nukleofil reakcióban, és a 2. ábra mutatja, hogy a rea-ció bimolekuláris, azaz, abban a lépésben, hogy meghatározza, a reakció sebesség .. egészben (ebben az esetben a kialakulása egy átmeneti álló-TION), az érintett két reaktánsok (halogenoalkane és nukleofil). Ez az arány a reakció zajlik a SN 2 mechanizmus koncentrációjától függ mindkét reaktáns.
SN 1 mechanizmus (monomolekuláris nukleofil szubsztitúció)
Ezzel a mechanizmussal, a nukleofil szubsztitúció a Thr - részecske és, bizonyos feltételek mellett, a szekunder halogén-alkánok. A molekula tercier halogénezett alkánok terjedelmes szubsztituensek a szén-atomok IU kapcsolódó halogénatom, hozzon létre térbeli pre-elzáródás a megközelítést a nukleofil a elektrofil központja, és a hátsó támadás lehetetlenné válik. Azonban, a tercier halo-alkánok képesek erősen poláris közegben ionizáció. Szerint mecha th SN 1 reakció zajlik két szakaszból áll:
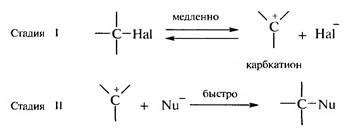
Az első lépésben a molekulák disszociál haloalkánban bevonásával protikus poláros oldószer-molekulákat. Az eredmény az újjáalakított karbokation és egy halogenid ion. Mivel a pro-lassú folyamat az ionizáció, a 1. lépésben meghatározza a reakció sebességét. Egy második lépésben a kapott karbokation gyorsan reagál a nukleofil.
A reakciót SN 1 mechanizmus elősegítik a magas ionizáló képesség és solvatiruyushaya oldószert és a stabilitást a kapott karbokation. Stabilitás alkil karbokationok miatt delokalizációja pozitív töltés miatt + I-hatása alkilcsoportok és növekszik a sorozat:
Ezért tercier halogénezett legegyszerűbb vetjük Xia ionizáció.
A mechanizmus a nukleofil szubsztitúciós, úgy véljük, az on-áramló rennoy nevű rendszer monomolekuláris, t lépéssel, a meghatározás hasadó sebessége a teljes folyamat (1. lépés) részt vesz mo-molekulák csak egy reagenst - .. halogénalkán. Egy ilyen mechanizmus a jelentős SN-1.
Így, az A fentiek alapján, arra lehet következtetni, hogy az elsődleges halogénalkánok általában reagálnak mechanizmus 2 Sn, tercier - SN mechanizmus 1. Másodlagos halogénalkánok, jellegétől függően a nukleofil, és az oldószer lehet körte-értelmezett, mint SN 2 mechanizmust, és az SN 1 mechanizmus.
1. lépés A halogénezett alkánok. Halogénezett alkánok hidrolizál Spear-ing. A reakciót általában a vizes oldatok jelenlétében, a rés-lochey, t. K. A víz ez lassú folyamat.
2. Williamson éter-szintézis. Ez a reakció az egyik legjobb nyílt forráskódú szoftverek sobov éterek előállítására. Ez a reakció a halogénezett alkánok alkoholátokkal vagy fenátok.
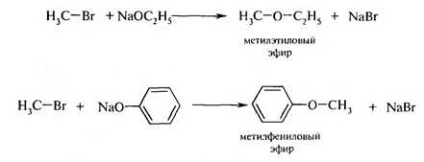
3. Kölcsönhatás karbonsav ömlesztősókat (acetolízist). Amikor dei következmény képzett karbonsav sók a halogénezett alkánok komplexitás-WIDE észterek. A reakciót aprotikus poláris szol-erator.
4. Kölcsönhatás ammóniával, alkil- és aril-aminok (ammonolízis és aminolízis). Ammóniával és aminokkal HN halogén-ezek alkilezett keverékét képezve a primer, szekunder és tre-részecske-aminok, valamint sóik - kvaterner ammónium-bázis-CIÓ. Például, a primer amin képződik, amelyeket a rendszer:
5. Kölcsönhatás sók tsianovodorodnoy savval. Primer és szekunder haloalkánok kálium- vagy nátrium-cianid jelenlétében, aprotikus poláros oldószerben, és így a nitrilek (SN 2):
6. Kölcsönhatás sói salétromossav. Termékek címzés-kötése egy e reakció eredményeként körülményeitől függ annak ráfordítás-CIÓ. szerkezete halogénalkánt és a sót.
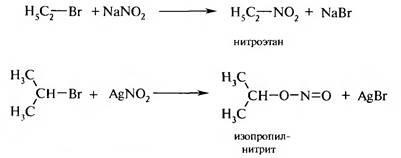
eliminációs reakciók kíséri hasításával halogének novodoroda haloalkán és kialakulásához vezet az alkének.
Mivel a hidrogén-absztrakciós bekövetkezik a # 946; szénatom, az ilyen reakciók nevezzük # 946; - vagy 1,2-eliminációs.
Lehasitjuk (E) és a nukleofil szubsztitúció (SN) versenyeznek egymással, de bizonyos körülmények között, mindegyik válhat domináns. A hasítási hidrogén-halogenid válik az elsődleges folyamat halogénaíkánnai jelenlétében NAA-leofilnyh reagensek biztosításával, amelyeknek nagy bázikus karakterének. Ezek közé tartoznak az alkoholos oldatokat, alkálifém-hidroxidok vagy alkálifém-alkoholátok. Hozzájárulás eliminációs így a hőmérséklet-emelkedés a reakcióelegy és a koncentráció ReA Gent. Így a reagáltatást jódetánnal vizes shelochi fő iránya a reakció egy nukleofil-schenie cserélni, és a reakcióterméket - etil-alkohol. Ha alkoholos lúgos oldatban válik domináns folyamatnak eliminációs reakció a reakció terméke - etilén.
Halogén-alkánok eliminációs reakció mehet végbe, MO nomolekulyarnomu (E1) és bimolekuláris (E2) mechanizmusok.
Mechanizmus E2 (bimolekuláris elimináció).
A hasítási reakció mechanizmusa E2 a legkönnyebben alávetni primer halogén-alkánok.
hasítási reakció által okozott bimolekuláris Mecha-mu, igényli bázis jelenlétében, az egy lépésben átmenetet képezve-egyen állapot, amelyben a fogadó képződését ESTATE távú molekula két reagenst. És ezért az arány egy ilyen reakció-lóg mindkét reakciópartner koncentrációját. szakadás folyamatok és a kialakulását Bani kötések az átmeneti állapotban van szinkron.
Ellentétben a SN 2 mechanizmus a mechanizmus az E2 részecske magányos elektronpár vagy negatív töltéshordozók nem jár, mint egy nukleofil, valamint egy bázis, a hidrogénatom a támadó # 946 szénatom.
E1 mechanizmus (monomolekuláris elimináció).
A legkönnyebben úgy jelentkezik megszüntetéséről mecha-edik pillanatban tercier halogénezett alkánok. A reakció olyan bázist igényel, mint egy reagens, de a természetesen megköveteli ionizáló coff-Tel. Ez egy kétlépéses eljárás.
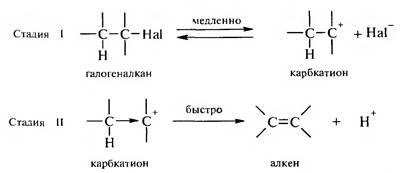
Meghatározási lépés a reakció sebessége, a kialakulását karbokation. A második szakaszban az stabilizálására szénkation kiküszöbölése révén a proton.
Ha a molekulában több alternatíva halogénalkán-CIÓ utak megszüntetése hidrogén-halogenid, akkor rájött, hogy az egyik, amelyben a kettős kötés a leginkább helyettesített szénatom, azaz halogénatommal ki hidrogén legalább hidrogénezett szomszédos szénatommal.
Ez a minta az úgynevezett Zajcev szabályok: